[연구동향]
Longitudinal change in dopamine transporter availability in idiopathic REM sleep behavior disorder
Neurology, 2020

파킨슨병은 고령화사회에서 유병율이 점점 증가하고 있는 난치성 뇌신경계 퇴행성 질환이다. 파킨슨병은 임상적으로 증상이 발현되기까지 수년에서 최장 20년까지도 긴 전구기를 가지고 있다. 이 전구기에 파킨슨병으로 진행하는 병태생리학적 기전을 밝히고 진행을 추적할 수 있는 바이오마커를 확립하는 것은 질병의 초기에 진행을 막는 궁극적인 치료제 개발을 위해서 필수적 과제가 되어 왔다. 이지영 교수가 주도하고 있는 보라매병원 파킨슨병 연구팀은 2013년부터 특발성 램수면행동장애 환자의 코호트를 만들어 전구 파킨슨병의 뇌신경계변화 및 임상적 징후를 분석해왔다. 특발성 램수면행동장애는 알파시누클린 응집이 있는 봉입체가 생기는 뇌신경계병리를 가지는 파킨슨병 및 루이소체치매의 전구단계에서 나올 수 있는 대표적 신경계질환이다.
연구팀은 핵의학과 김유경 교수팀과 함께 PET/CT를 이용하여 뇌 도파민 신경계 말단의 표지자인 도파민 운반체의 정량적 분포와 변화를 이 파킨슨전구기 코호트에서 측정하였다. 비교분석 대상은 연령을 짝지은 정상인과 램수면행동장애가 선행하다가 처음 파킨슨병을 진단받은 초기 파킨슨병 환자들의 데이터였다. 이 영상데이터를 면밀히 비교 분석함으로써, 램수면행동장애 환자들이 건강한 상태와 파킨슨병이 나타난 상태의 중간 수준에 해당하는 도파민 운반체 감소를 가지고 있음을 뇌 흑질과 선조체 각 영역에서 정량적으로 보여주었다. 이로써 파킨슨전구기로서의 램수면행동장애의 발현에 대한 기존의 병리학적 가설을 뒷받침하였다.
또한, 연구팀은 이 램수면행동장애 코호트를 5년 이상 추적 관찰하면서 임상적 징후의 진행 양태를 신경학적 척도를 통해서 정량화하고, 2년 및 4년 시점에 얻은 도파민 운반체 영상을 추가적으로 분석하여 그 변화량을 측정함으로써, 전구 파킨슨병에서 나타나는 도파민 신경계의 퇴행 속도와 임상적 징후의 출현 및 진행과의 상관성을 전향적으로 추시할 수 있었다. 이번에 출판한 논문에서는 램수면행동장애 환자에서 전구 파킨슨병의 징후들 중, 특히 후각저하 유무가 도파민 신경계 퇴행정도를 예측하고 (그림 1), 이 징후와 도파민 운반체의 변화를 통합적 바이오마커로 해석하면, 향후 2년 이내 파킨슨병 및 루이소체치매로 진행하는 확률도 유의하게 예측할 수 있다는 사실(그림 2)을 한국인 데이터를 이용한 전향적 분석으로 보여주었다. 또한, 정량화한 뇌 기저핵 각 영역 도파민 운반체 영상 자료를 주성분 분석 (Principal Component Analysis) 방법으로 새롭게 해석함으로써(그림 2), 파킨슨전구기 환자 개개인에서 질병 진행 위험도를 간단한 수치로 보여줄 수 있는 방법을 함께 제시하였다. 이 주성분 분석으로 얻은 도파민 운반체의 패턴 z-환산점수는 매년 파킨슨병으로 진행함에 따라 점점 파킨슨병 패턴으로 변화하고, 이 변화속도를 1차 결과변수로 잡을 경우 임상시험에 필요한 총 연구대상자수를 현실적 수준으로 낮출 수 있음을 보여주었다. 이로써, 본 연구진은 전구파킨슨기 치료제 개발을 위한 임상시험모델을 이론적 상태에서 현실가능한 상태로 한단계 앞당길 수 있는 획기적인 아이디어를 제공하였다. 이 연구 결과물은 알파시누클린병증으로서의 램수면행동장애의 병태생리학적 이해 수준을 높이고, 향후 파킨슨병 극복을 위한 신경보호치료제 개발에 유용한 바이오마커로 활용될 것이다.


Induction of the IL-1RII decoy receptor by NFAT/FOXP3 blocks IL-1β-dependent response of Th17 cells
Elife, 2021

1970년대 초 내인성 발열인자로 발견된 인터류킨-1(IL-1)은 IL-1α와 IL-1β로 구분되며 염증반응과 숙주방어기전에 핵심적인 사이토카인이다. IL-1로 매개되는 광범위하고 강력한 염증반응을 정교하게 조절하고자 세포는 복잡한 IL-1 수용체(IL-1R) 시스템을 활용하여 알려졌다. 새로운 사이토카인들이 다수 발견되면서 IL-1에 대한 관심이 다소 떨어져가고 있었으나, IL-1β를 활성화시키는 inflammasome 발견(2002년)과 자가면역질환을 유발하는 Th17 분화에 IL-1β이 직접적으로 관여한다는 보고(2007년)를 통하여 다시 면역학자들의 큰 주목을 받게 되었다.
본 연구는 인간 CD4+ T세포에서 IL-1 수용체의 발현과 그 조절 기전, 그리고 면역학적 의의를 보고한 이전 연구(Lee WW, Blood, 2010)의 연장선상에서, 당시 풀지 못했던 주요한 질문에 대한 답을 내고자 노력했던 김동현 박사과정생[단독 제1저자; Laboratory of Autoimmunity and Inflammation (LAI)]과 공동연구자들의 산물이다.
자가면역질환을 유발하는 병인성 Th17세포 반응에 IL-1β가 매우 중요하지만 IL-1β 신호전달에 필요한 IL-1 수용체가 어떻게 발현, 조절되는지는 자세히 알려지지 않았다. 본 연구에서는 대표적 IL-1 수용체(functional IL-1RI, decoy IL-1RII) 중 IL-1RII가 일부 IL-1RI+ CD4 T세포에서 발현하고 IL-1β신호를 미세조정하여 병인성 Th17 면역반응을 조절함을 인간 CD4 T세포를 활용하여 밝혔다. 또한 NFAT과 Foxp3가 상호작용에 의해 직접적으로 조절되는 IL-1RII 발현 기전을 최신 분자면역학적 기법으로 규명하였다. IL-1RII를 발현하는 Th17 세포는 Treg (조절 T세포)과 유사한 특성을 나타내며 과도한 면역반응을 억제하는 데 관여하였다. 이러한 IL-1RII 발현은 류마티스 관절염환자의 말초혈액 및 관절활액 내 CD4+ T세포에서 현저히 감소하였고, 이는 병인성 Th17 반응 강화와 연관되어 있다.
이번 연구로 얻어진 결과는 decoy 수용체 IL-1RII의 발현기전을 새롭게 규명하고, IL-1RII를 발현하는 Th17세포의 잠재적 면역조절 기능을 확인하였다는 점에서 의미가 있으며, 매년 증가하고 있지만 근원적인 치료법 개발은 아직 요원한 실정인 난치성 자가면역질환의 새로운 치료 접근방법으로 활용될 수 있을 것으로 기대된다.

Discovery of molecular features underlying the morphological landscape by integrating spatial transcriptomic data with deep features of tissue images
Nucleic Acids Research, 2021

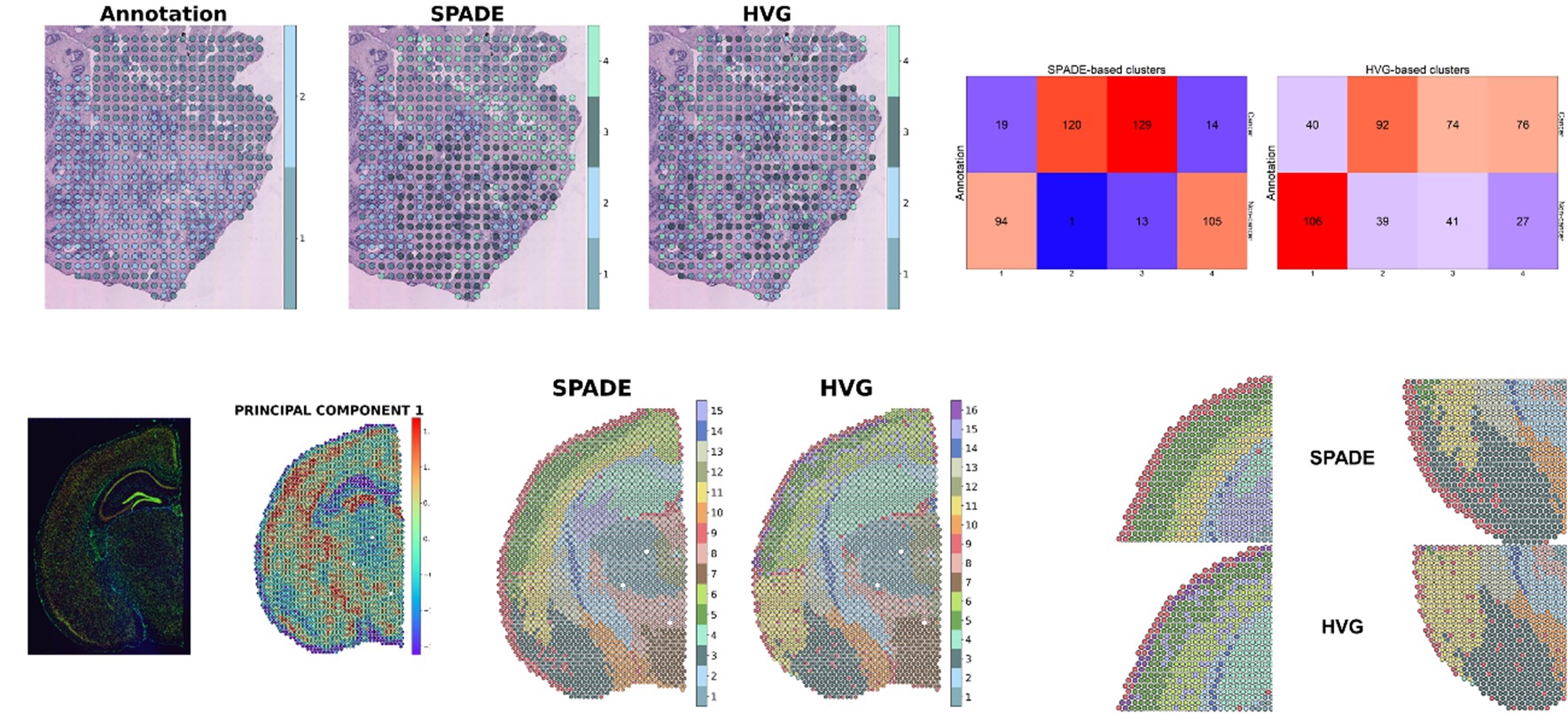
공간 전사체 기술은 정밀한 수준의 전장유전자의 발현정보를 공간적정보를 포함하여 획득하는 최신 기술이다. 이러한 공간전사체 기술은 다양한 질환에 적용되어 질병의 병태생리를 이해하고 새로운 치료 타겟을 발굴하며 진단적 바이오마커를 발굴하는데 널리 활용이 기대되고 있다. 하지만, 이러한 대규모의 복잡한 데이터를 해석하여 임상적으로 이어질 수 있는 해석방법의 개발이 필요한 상황이다. 핵의학과 연구팀은 이러한 공간전사체 데이터가 공간정보가 함께 있다는 점에서 이미지데이터와 접목하여 해석할 수 있다는 점에 주목하여, 통합하여 해석하는 방법을 개발하였다.(그림 1).
본 연구에서는 조직 이미지로부터 딥러닝 기술을 통해 이미지의 주요한 특성을 수치화된 값으로 획득하고, 이와 관련된 유전자 발현 정보를 획득하는 새로운 기술을 제안하였다. 그 결과, 조직의 구조적인 특성과 연관된 분자적 특성을 가설이나 기존 정보 없이 획득할 수 있었으며, 조직 이미지 특성과 연관성 높은 유전자를 모아서 클러스터링을 진행한 결과, 종양조직이나 뇌의 기능적 영역을 잘 반영할 수 있음을 보였다 (그림 2). 특히, 활용되는 이미지는 공간적 정보와 통합이 가능한 종류라면 (형광이미지, Autoradiography 이미지 등) 함께 접목이 가능하여, 공간 기반 멀티오믹스 분석으로 발전할 수 있을 것이다. 본 연구에서는 공간적 정보까지 더해진 수많은 영역의 유전자발현 데이터를 이미지 정보와 함께 통합하여 해석할 수 있는 기술을 제공함으로써, 새로운 질병의 병태생리를 찾거나 질병에 적합한 치료 타겟을 발굴하기 위한 다양한 분야로 적용될 수 있을 것이 기대된다.

논문링크 : https://academic.oup.com/nar/advance-article/doi/10.1093/nar/gkab095/6146632
Disease-specific eQTL screening reveals an anti-fibrotic effect of AGXT2 in non-alcoholic fatty liver disease
Journal of Hepatology, 2021

지방간질환은 전체 한국인 중 약 25%에서 발현되는 주요 대사질환으로서 질환이 진행될 경우 지방간염, 간경화, 간암 등의 심각한 말기 간질환으로 악화될 가능성이 높고, 다른 연관 대사질환들 (당뇨병, 고혈압, 심혈관질환, 만성콩팥질환 등)의 발병 위험도 크게 증가시키는 것으로 알려져 있다. 그러나 지방간질환에 대해 지금까지 임상에서 승인된 약제는 없는 것으로 알려져 있는데, 그 주요 실패 원인으로 그동안의 지방간질환 신약 개발 임상시험들은 환자들의 임상적, 유전적 다양성을 고려하지 않았다는 점이 지목되었고 이를 극복하기 위한 혁신적 환자 맞춤형 정밀 표적 신약 개발의 필요성이 지속적으로 제기되어 왔다.
본 연구팀은 최근 지방간 네트워크 ITEN (Innovative Target Exploration of NAFLD) 컨소시엄 공동연구를 통해 비알코올 지방간질환에서 환자 맞춤형 정밀의료 신약 개발과 관련하여, 비알코올성 지방간 질환 환자 125명의 유전자 발현 정보와 유전체 정보를 통합 분석하여 환자 맞춤형, 질병 특이적 eQTL (expression quantitative trait loci) 알고리즘을 고안하였다. 이를 통해 특정 유전형을 가진 환자들이 지방간질환 조직에서 간 유래 특정 유전자 발현을 조절한다는 가설을 증명하였고 그 결과 AGXT2라는 유전자가 지방간질환 유발에 중요한 인자임을 주목하고 이를 세포/동물 모델과 인체 데이터에서 증명하였다. 이는 AGXT2 발현을 조절하는 특정 유전 변이를 가지고 있는 지방간 환자에게서만 특이적으로 일어나는 유전자 발현을 예측함으로써 환자 맞춤형 정밀진단 및 표적치료의 획기적인 돌파구를 마련할 것이라는 점에서 혁신적인 의미를 갖는다고 할 수 있다.

논문링크 : https://www.journal-of-hepatology.eu/article/S0168-8278(21)00246-4/abstract
Prasugrel-based de-escalation of dual antiplatelet therapy after percutaneous coronary intervention in patients with acute coronary syndrome (HOST-REDUCE-POLYTECH-ACS): an open-label, multicentre, non-inferiority randomised trial
Lancet, 2020
 김효수 교수
김효수 교수(내과학교실)
 박경우 교수
박경우 교수(내과학교실)
 강지훈 교수
강지훈 교수(서울대학교병원 내과학과)
관상동맥 중재시술은 협심증 및 심근경색의에 대한 치료로 시행되고 있으며, 이후의 약물치료도 환자의 장기예후에 매우 중요하다. 약물 치료법 중, 특히 항혈소판제의 사용은 관상동맥 중재시술 이후 발생하는 혈전성 부작용을 예방하는데 큰 역할을 하지만, 출혈성 부작용을 일으킬 수 있기 때문에 적절한 용법으로 사용하는 것이 중요하다. 현재 가이드라인에서는 관상동맥 중재시술 이후 6~12개월 동안 이중항혈소판요법 (Dual antiplatelet therapy)를 추천하고 있으며, 급성관동맥증후군 (acute coronary syndrome) 환자의 경우 보다 강한 항혈소판제 (potent P2Y12 inhibitor)를 권장하고 있다. 다만, 기존의 가이드라인은 주로 서양인을 대상으로 한 연구를 대상으로 설정되었을 뿐만 아니라, 관상동맥 중재시술 이후 발생하는 혈전성 위험성과 출혈성 위험성의 시간적 변화 (temporal change)를 반영하지 못하고 있다. 즉, 관상동맥 중재시술 직후에는 혈전성 위험성이 상대적으로 높기 때문에 강한 항혈소판제가 필요하고, 만성기에는 출혈성 위험성이 보다 높아지기 때문에 보다 약한 항혈소판제를 사용해야 혈전성 부작용과 출혈성 부작용을 최소화할 수 있다. 특히, 출혈성 이벤트이 많이 발생하는 동양인에서는 만성기에 항혈소판제의 강도를 낮추는 단계적축소 (de-escalation) 전략이 보다 유용할 수 있다.
본 연구에서는 관상동맥 중재술을 시행받은 한국인 급성관동맥증후군 환자에서 항혈소판제의 단계적축소 전략의 유효성과 안전성을 평가하였다. 연구자 주도 임상시험으로 2011년부터 고안하여 준비하였고 2014년부터 환자 등록을 시작하여 국내 35기관에 총 2338명의 환자들이 등재되었으며, 단계적축소군 (de-escalation group; n=1170) 혹은 통상치료군 (conventional group; n=1168) 으로 무작위배정되었다. 관상동맥중재술 이후 1년 동안 추적관찰한 결과, 1차 평가 변수 (사망, 심근경색, 스텐트혈전증, 재혈관술, 뇌졸중, 출혈)의 발생율이 단계적축소군에서 7.2%, 통상치료군에서 10.1% 였으며, 항혈소판제의 단계적축소 전략이 유의하게 이벤트가 줄일 수 있음을 보였다 (Hazard ratio 0.70 [95% CI 0.52-0.92], p=0.012; 그림). 본 논문의 연구 결과를 바탕으로, 관상동맥 중재술 후의 항혈소판제 사용 전략에 있어서 단계적축소 전략의 유효성과 안전성을 증명할 수 있었으며, 우리나라 급성관동맥증후군 환자에서 항혈소판제 사용의 가이드라인을 제시할 수 있을 것으로 기대한다.
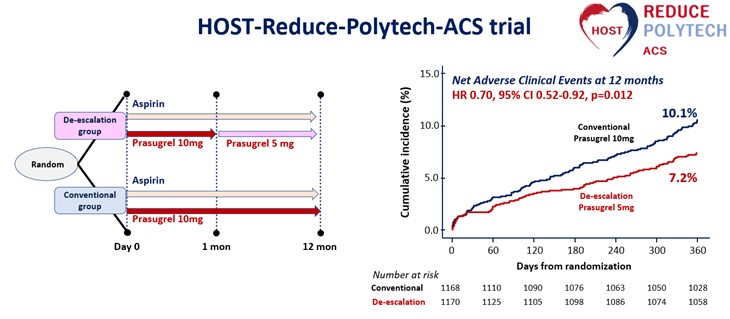
그림. HOST-REDUCE-POLYTECH-ACS 연구의 흐름 및 1차 평가 변수 결과
논문링크 : https://www.thelancet.com/article/S0140-6736(20)31791-8/fulltext

