[연구동향]
Simultaneous detection of neural activity and temperature in photothermal neural stimulation
Advanced Science

(의공학교실, 교신저자)

(의공학교실, 공동제1저자)
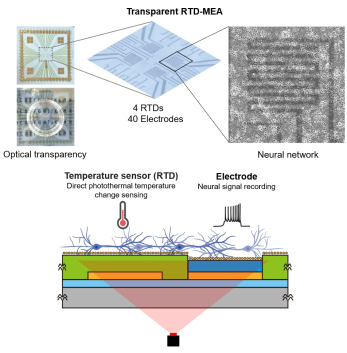
광열 신경 조절 기술은 뇌의 신경 회로를 연구하고 신경 질환을 치료하는 유망한 방법이다. 이 기술은 유전자 변형 없이 빛을 이용해 뇌 신경 활동을 조절할 수 있는 가능성을 가지고 있으며, 특히 뇌전증이나 발작과 같은 신경계 질환 치료에 도움이 될 수 있다. 이 기술의 핵심은 플라즈모닉 나노 소재를 활용해 세포막 근처의 온도를 순간적으로 올리는 것이다. 이렇게 온도가 변하면, 세포막의 물리적 성질이 달라지거나 온도에 반응하는 특정 이온 채널이 열리고 닫히면서 신경세포의 활동을 조절한다. 온도 민감성 이온 채널은 열 자극을 전기 신호로 변환하는 역할을 하며, 이는 신경 조절 기술이 작동하는 데 중요한 요소이다. 지금까지의 광열 신경 조절 연구는 광학 자극 중 신경 세포 표면의 온도 변화를 직접 측정할 수 없기 때문에 신경 신호 측정 중 광열 자극에 의한 온도 변화를 알기 어려웠다. 또한 기존의 온도 측정 방법들은 정확도가 부족하거나 빛 간섭에 의해 온도 측정에 어려움을 겪고 있어, 광열 신경 자극에 의한 세포 표면 온도를 실시간으로 정밀하게 측정하는 투명 온도 센서 기술이 필요하였다.
본 연구에서는 세포막의 온도 변화와 전기 신호를 동시에 측정할 수 있는 투명 저항 온도센서(transparent resistive temperature detector, tRTD)와 다채널 투명 전극 어레이(microelectrode array, MEA)를 결합한 시스템을 개발하였다. 이 시스템은 10 nm 두께의 초박형 금(gold) 박막으로 구성된 투명 전극과 온도 센서를 제작하여, 뛰어난 전도성, 투명성, 생체 적합성을 제공하였다. 추가적인 플라즈모닉 금 나노 섬(gold islands) 구조와 투명 전도성 고분자(PEDOT: PSS)층은 전극이 보다 우수한 전기화학적 특성을 유지하면서 근적외선(NIR) 빛으로 광열 효과를 구현할 수 있도록 하였다. 제안된 tRTD-MEA 시스템은 신경 세포 배양 조건에서 세포 표면의 온도 변화를 약 0.06 °C 해상도 수준으로 정확하게 관찰할 수 있으며, 광열 신경 억제 자극을 통한 신경 기록 및 광학 이미징을 성공적으로 수행했다. 그 결과 세포막 근처에서 약 2.3°C의 온도 증가가 일어나면 신경세포의 활성이 약 95%까지 억제될 수 있음을 확인하였다. 또한 신경 세포의 마이크로 스케일에서 온도 변화를 직접 측정하는 것은 신경 질환 치료 방법을 개발하는 데 중요한 지표가 될 것이다.

Association of cholecystectomy with short-term and long-term risks of depression and suicide
Scientific Reports

(가정의학교실, 교신저자)

(의과학과, 공동제1저자)

(의과학과, 공동제1저자)
담낭절제술은 주로 담석 질환을 치료하기 위해 시행하며 담낭을 제거하는 수술로 비교적 안전한 수술로 알려져 있다. 그러나 최근 연구에서는 담낭절제술이 소화기 암, 대사 질환 등 다양한 건강 결과와 관련이 있음이 밝혀졌다. 담낭절제술과 심혈관질환, 대사 지표 간의 연관성을 확인한 선행 연구에 따르면, 담낭절제술이 심혈관질환 위험을 증가시키거나 대사 건강을 개선하는 경우도 있었다. 이처럼 담낭 제거 후 건강 결과에 대한 논란이 여전히 존재한다. 담낭절제술 후 일부 환자는 우울 및 불안과 같은 정신 건강 문제와 관련이 있을 수 있지만 담낭절제술이 장기적으로 우울증 위험을 증가시키는지에 대한 연구는 부족하다. 또한, 한국의 자살률이 높은 상황에서 담낭절제술 후 자살 위험과의 연관성은 충분히 연구되지 않은 실정이다.
본 연구는 2002년부터 2019년까지 담낭절제술을 받은 40세 이상의 성인을 대상으로 한 한국의 국민건강보험 건강검진 코호트(NHIS-HEALS)의 데이터를 분석하였다. 총 6,688명의 담낭절제술 환자와 연령 및 성별을 1:10으로 매칭한 대조군을 비교하여 담낭절제술과 우울증 및 자살 위험 간의 연관성을 평가하였다. 우울증 및 자살 발생 여부는 수술 후 3년 이내를 단기 위험(short-term risk), 3년 이후를 장기 위험(long-term risk)으로 구분하여 수술 날짜부터 2019년 말까지 추적하여 국내의 담낭절제술 환자 대상으로 우울증 및 자살 간의 연관성을 보다 심층적으로 파악하고자 하였다.
담낭절제술과 우울증 및 자살 위험 간의 연관성을 분석한 결과, 담낭절제술을 받은 그룹은 그렇지 않은 그룹에 비해 단기적으로 우울증 발생 위험이 약 38% 증가한 것으로 나타났다(조정된 위험비 [aHR]: 1.38, 95% CI: [1.19-1.59]). 그러나 수술 후 3년 이후 장기적인 우울증 위험은 유의하게 증가하지 않았다([aHR]: 1.09, 95% CI: [0.98-1.22]). 또한, 자살 위험과의 연관성은 통계적으로 유의하지 않았다([aHR]: 1.08, 95% CI: [0.69-1.68]). 하위 그룹 분석에서도 연령, 성별, 동반 질환 여부에 관계없이 단기적인 우울증 위험 증가 경향이 유사하게 관찰되었다.
본 연구는 담낭절제술 환자의 수술 후 마음 건강 관리에 관한 임상 근거를 제공하는 데 중요한 역학적 근거를 제공한다. 더불어 담낭절제술과 우울증 및 자살 간의 관계를 확인함으로써 임상의가 환자의 장기적인 건강 상태를 보다 효과적으로 관리할 수 있도록 돕고 관련 공중 보건 전략 개발에도 기여할 수 있을 것으로 기대된다.

Healthy lifestyle reduces cardiovascular risk in women with genetic predisposition to hypertensive disorders of pregnancy
Nature Communications

(산부인과학교실, 공동교신저자)
본 연구는 서울대학교 의과대학 산부인과학교실 이승미 교수 연구팀과 University of Pennsylvania, Department of Biostatistics 김도균 교수 연구팀이 공동으로 수행한 연구로, 대규모 유전체 데이터를 활용하여 임신 중 고혈압 질환(HDP)에 대한 유전적 위험과 동맥경화성 심혈관 질환(ASCVD) 발생 위험에 대한 연관성을 평가한 연구이다.
HDP는 여성의 장기적인 ASCVD 위험을 증가시키는 중요한 요인으로 알려져 있다. 최근 연구들은 HDP의 유전적 위험이 ASCVD 발생과 연관이 있음을 시사하지만, 생활습관 및 대사 건강이 이러한 위험을 완화할 수 있는지에 대한 연구는 부족하다. 이에 본 연구는 대규모 유전체 분석 데이터를 이용하여 HDP 유전적 위험과 ASCVD 발생 간의 관계를 평가하고, 건강한 생활습관과 대사 건강 상태가 ASCVD 예방에 미치는 영향을 분석하였다.
연구는 UK Biobank (164,500명)와 Penn Medicine Biobank (2,001명)의 데이터를 이용하여 진행되었다. HDP에 대한 유전적 위험은 대규모 GWAS 데이터를 기반으로 다유전자 위험 점수(PRS)로 평가되었으며, 생활습관 및 대사 건강 상태(대사 증후군 요인 등)가 ASCVD 발생에 미치는 영향을 다변량 Cox 회귀 분석을 통해 분석하였다.
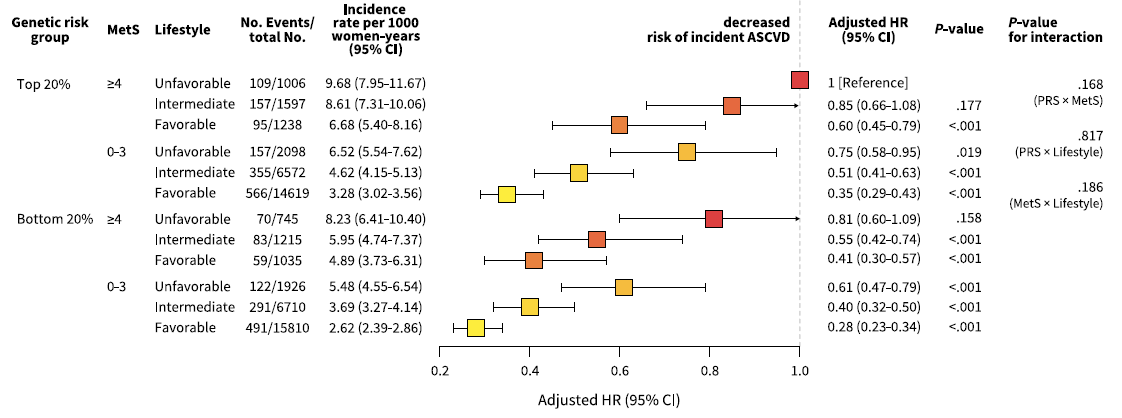
분석 결과, HDP에 대한 유전적 위험이 높은 여성은 낮은 유전적 위험군보다 ASCVD 발생 위험이 증가하였다(HR 1.47 (1.18–1.83)). 그러나 건강한 생활습관(비흡연, 정상 체중, 규칙적 운동, 균형 잡힌 식단)과 이상적인 대사 건강 상태를 유지할 경우, ASCVD 위험이 최대 64.6%까지 감소하였다. 특히, 높은 유전적 위험군에서도 건강한 생활습관을 실천한 경우 위험 감소 효과가 뚜렷하게 나타났다.
본 연구는 유전적 요인이 ASCVD 위험을 증가시키지만 건강한 생활습관이 이를 효과적으로 완화할 수 있음을 입증하였다. 특히 유전적 위험이 높더라도 적절한 생활습관과 대사 건강 관리를 통해 ASCVD 발생을 줄일 수 있으므로 개인 맞춤형 예방 전략이 필요하다. 향후 연구에서는 다양한 인종 및 지역을 대상으로 유사한 분석을 진행하여 결과의 일반화 가능성을 평가할 필요가 있다.
Aberrant ERK signaling in astrocytes impairs learning and memory in RASopathy-associated BRAF mutant mouse models
The Journal of Clinical Investigation

(생리학교실, 공동교신저자)

(의학연구원, 공동제1저자)
본 연구는 서울대학교 의과대학 이용석 교수와 연세대학교 의과대학 김철훈 교수로 구성된 공동연구팀이 희귀난치성 발달질환인 ‘심장-피부-얼굴 증후군’에서 발생하는 학습 및 인지 장애 원인을 규명한 연구이다.
심장-얼굴-피부 증후군(Cardio-facio-cutaneous syndrome)은 약 810,000명 중 한 명 꼴로 나타나는 희귀난치성 발달질환으로, 대부분의 환자들에게서 학습 장애를 포함하는 인지 기능의 장애가 나타나는 것으로 알려져 있다. 하지만 이처럼 높은 비율에 비해 그간 심장-얼굴-피부 증후군과 연관된 인지 기능 장애의 신경생물학적 기전에 대한 연구는 거의 이루어지지 않았고, 따라서 이에 대한 치료법은 전무한 실정이다.
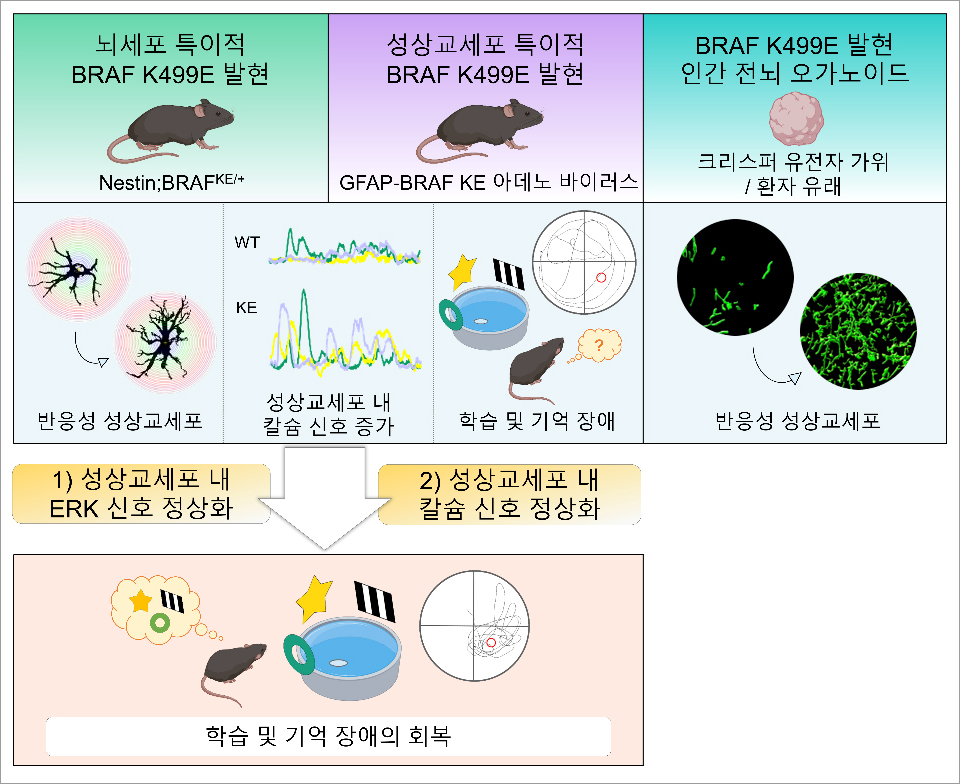
본 연구팀은 마우스 모델과 환자 유래 줄기세포를 이용하여 뇌 세포 중 한 종류인 성상교세포의 비정상적인 과활성화가 심장-얼굴-피부 증후군에서 나타나는 인지 장애의 원인임을 새롭게 밝혀냈다. 심장-얼굴-피부 증후군 유발 돌연변이인 BRAF K499E를 뇌세포 전반에 발현시킨 쥐의 피질 및 해마 부위에서 반응성 성상교세포 마커의 발현이 증가했으며, 이로 인해 성상교세포의 형태가 비정상적으로 비대해지는 것이 확인되었다. 형태적 이상과 더불어 기능적 이상을 확인하기 위해 뇌 조직에서 2광자 칼슘 이미징 기술로 세포 내 칼슘 신호를 측정했을 때, 돌연변이 생쥐의 성상교세포 칼슘 신호 역시 비정상적으로 증가했다.
아데노 바이러스를 이용해 성상교세포에만 특이적으로 BRAF 돌연변이를 발현시켰을 때도 마찬가지로 반응성 성상교세포의 증가 및 칼슘 신호 과활성, 그리고 학습 장애가 나타났다. 마지막으로, BRAF 돌연변이 생쥐 모델에서 과도하게 증가되었던 성상교세포 내 칼슘을 인위적으로 낮추어 정상화시켰을 때 학습 및 기억 장애가 회복되는 것을 확인함으로써, 성상교세포의 이상이 심장-얼굴-피부 증후군 연관 인지 장애의 병리 기전임을 밝혀냈다.
본 연구는 기초과학적 측면에서 성상교세포 칼슘 신호 조절에 BRAF 단백질이 중요한 역할을 수행함을 발견하였으며, 향후 성상교세포를 표적으로 하는 신경발달질환 치료전략 개발 가능성을 제시한다.
On-patient medical record and mRNA therapeutics using intradermal microneedles
Nature Materials

(의공학교실, 공동제1저자)
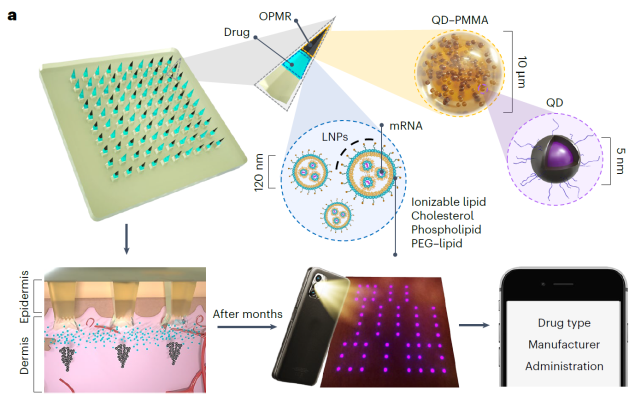
mRNA 백신을 포함한 약물 및 치료는 일정한 간격을 두고 투여해야 하는 일련의 투약이 필요하며, 이를 위해 정확한 의료 기록 관리가 필수적이다. 따라서, 의료 기록이 잘 관리되지 않는 지역이나 진료 현장에서는 치료 효과가 감소하거나 질병 예방이 어려워지는 문제가 발생한다.
본 연구진은 mRNA 백신 마이크로니들에 퀀텀닷(quantum dot)을 암호화된 패턴의 형태로 추가하여 백신 접종 시 관련 의료 정보를 환자 피부에 직접 기록 및 출력하는 ‘on-patient medical record (OPMR)’ 시스템을 개발했다. 정확한 의료 정보를 전달하고 보존하기 위해 근적외선 발광 소재인 퀀텀닷을 poly (methyl methacrylate) (PMMA) 및 poly (lactic-co-glycolic acid) (PLGA) 와 같은 고분자로 캡슐화하여 생체 적합성과 입자 크기를 향상시키고, 마이크로니들의 높이, 각도, 간격 등의 디자인 요소를 최적화했다. 결과적으로, 퀀텀닷으로 이루어진 정보를 균일한 침투 깊이와 밝기로 진피층에 전달했다.
또한, 시간이 경과함에 따라 인체 내 퀀텀닷 발광 효율 감소 및 다른 외부적 요인으로 인한 정보 출력 오류를 방지하기 위해 오류 정정 코드(error correcting code)와 딥 러닝(deep learning) 기술을 접목하여 정확한 정보 입력 및 출력 시스템을 구현했다. 65만 개의 합성 패턴 이미지를 훈련 세트로 사용하여 이미지 정정 및 인식 네트워크 모델을 훈련시키고, 이를 통해 21개의 마이크로니들 패치를 3마리의 돼지에 in vivo 투여했을 시 3개월 동안 100%의 성공률로 패턴을 인식하고 출력하는 것을 확인했다. 마지막으로, 퀀텀닷과 SARS-CoV-2 mRNA 백신을 마이크로니들 패치에 co-loading 하여 쥐에 동시 투여했을 시 근육주사로 접종되는 기존 COVID-19 백신과 동일한 효과를 나타내는 것을 확인했다.
이 기술은 의료 기록 관리가 어려운 지역 환경에서 유용하여 글로벌 의료 형평성을 증진하고, 팬데믹과 같은 응급 현장에서 의료진이 보다 정확한 치료 결정을 내릴 수 있도록 도울 수 있다.