[연구동향]
Prospective phase II study of allogeneic hematopoietic stem cell transplantation with targeted busulfan, fludarabine, and etoposide conditioning in pediatric acute lymphoblastic leukemia
HemaSphere

(소아과학교실, 교신저자)

(의학과, 제1저자)
소아청소년에서 가장 많이 발생하는 혈액암인 급성림프모구백혈병은 많은 경우 약물 치료만으로 완치할 수 있으나, 재발하거나 초기 치료에 불응하는 경우 그리고 몇몇 최고위험군의 특성을 가진 환자의 경우는 더 나은 치료를 위해 동종 조혈모세포이식이 필요하다. 여전히 전신 방사선 조사를 이용한 조혈모세포이식이 더 좋은 치료 결과를 보이고 있으나, 전신 방사선으로 인한 다양한 장기 합병증이 성장과 발달을 하는 소아청소년 환자에게는 장기적으로 우려가 되는 점이 많은 것이 사실이다.
이에 방사선을 제외하고 약물만을 이용한 조혈모세포이식 관련하여 많은 연구가 진행되어 왔고, 서울대학교어린이병원 소아청소년과 강형진, 홍경택 교수팀은 개인별 적정용량의 항암제(부설판, Busulfan)를 이용한 동종 조혈모세포이식치료의 성공적인 전향적 임상시험 결과를 발표했다.
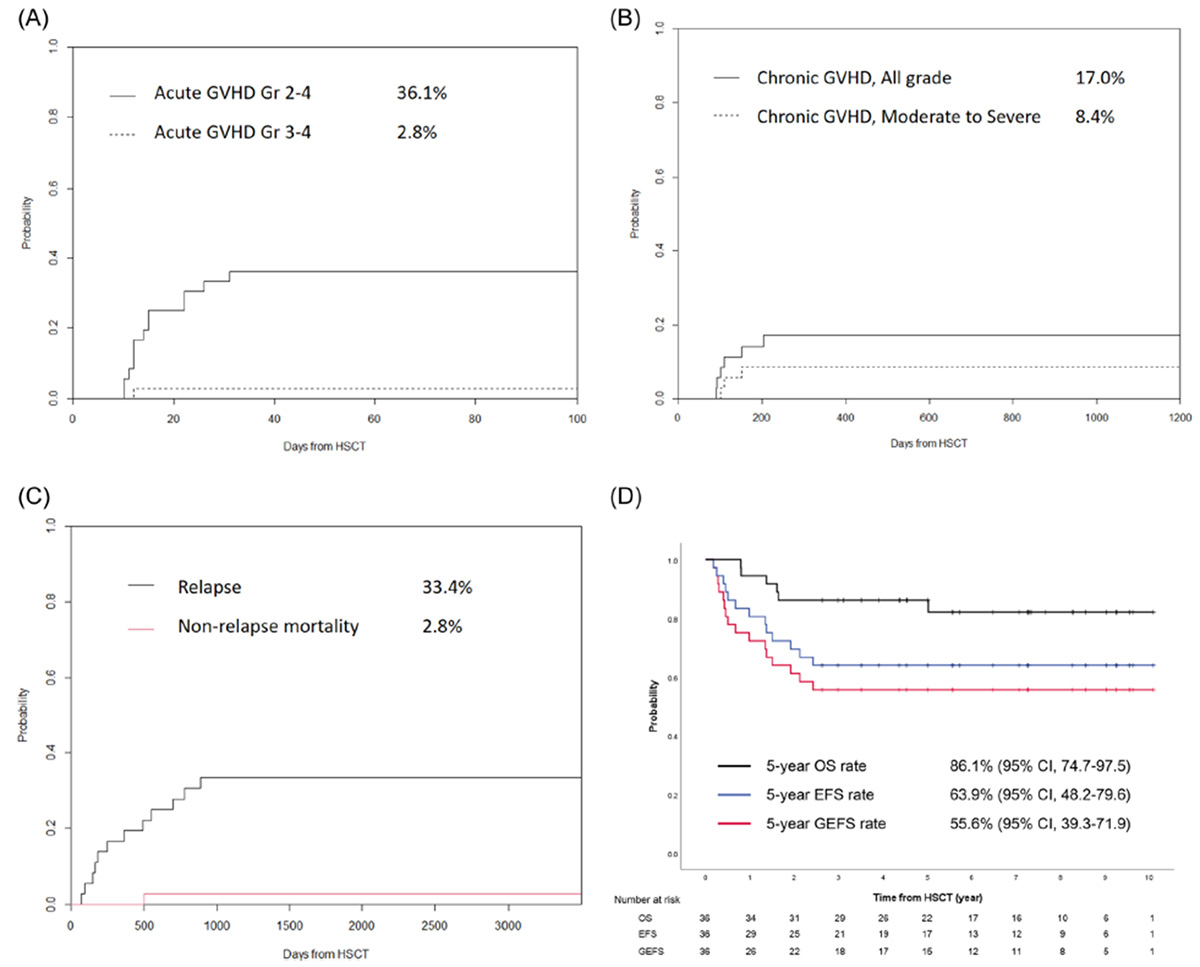
36명의 환자들이 부설판, 플루다라빈, 에토포시드라는 항암제를 이용한 전처치요법을 시행받았으며 전체 환자의 5년 생존율이 86%, 무사건 생존율은 64%로 확인되었다.(현재 국제 이식등록기관에서 발표한 소아청소년 급성림프모구백혈병의 혈연, 비혈연 공여자 조혈모세포 이식 성적은 질환 중증도에 따라 3년 생존율이 62-79%로 보고된다.) 또한 중증 급성 또는 만성 이식편대숙주반응도 2.8%, 8.4%로 기존 이식과 비교해 비슷하거나 더 나은 결과를 보였다. 특히 이번 연구 결과에서는 치료 관련 사망률이 2.8%로 매우 낮아 최근 유럽에서 진행된 FORUM 연구에서 약물만을 이용한 조혈모세포이식의 2년 생존율 75%보다 더 좋은 결과를 보였다.
최근에는 CAR-T 등의 다양한 면역세포치료들도 발전하고 있기에, 본 연구를 통해 소아청소년의 장기합병증을 고려하여 위험도에 따라 선별된 환자들에게 방사선을 제외한 조혈모세포이식을 시행할 수 있는 의미 있는 근거를 도출했다.
Differentiating visceral sensory ganglion organoids from induced pluripotent stem cells
Nature methods

(생화학교실, 공동교신저자)

(생화학교실, 공동교신저자)

(의과학과, 공동제1저자)

(의과학과, 공동제1저자)
2400년 전(기원전 약 400년) 고대 그리스의 히포크라테스는 “모든 질병은 장에서 비롯된다.”라는 격언을 남겼다. 의학자 히포크라테스의 관점은 최근까지도 이어지고 있다. 그 대표적인 것이 장-뇌 축이다. 장-뇌 축이란 장과 뇌가 서로 밀접하게 연관되어 있다는 의미를 지닌다. 최근 여러 신경계 질환의 발생 또는 악화를 장-뇌 축을 통해 설명하려는 시도들이 많이 이루어지고 있고, 30종류가 넘는 임상 시험이 장-뇌 축을 통하여 신경계 질환을 치료하고자 도전하고 있다. 이런 대부분의 시도들은 장과 뇌가 서로 소통하는 연결다리로 혈액을 지목한다(장-혈액-뇌 축). 그러나 혈액의 경우 뇌는 혈액-뇌 장벽이라는 강력한 방어벽이 존재하여, 혈액이 뇌에 미칠 수 있는 영향은 제한적이다. 이러한 혈액-뇌 장벽을 우회하는 지름길이 장과 뇌 사이에 하나 존재하는데, 이는 바로 미주신경(vagus nerve)이다. 미주신경은 장과 뇌를 직접 연결하며, 내장 감각 신경(visceral sensory neuron, VSN)과 내장 운동 신경(visceral motor neuron)으로 이루어져 있다. 이 중 내장 감각 신경은 장에서 발생한 신호를 뇌에 전달하고, 내장 운동 신경은 뇌에서 출발한 명령을 직접 장에 전달해주는 역할을 한다(장-신경-뇌 축).
최근 동물실험 연구들에서 이러한 미주신경이 파킨슨병, 알츠하이머병 같은 퇴행성 신경 질환에서 뇌 내에 폐기물처럼 쌓이게 되는 병적 단백질인 아밀로이드 베타, 타우, 알파 시누클레인 같은 물질들이 장에서 발생하여 미주신경을 타고 뇌로 전달될 수 있음을 밝힌 바가 있다. 이러한 동물실험 연구의 한계점은 생물체인지라 혈액이 존재하기 때문에 순수하게 장-신경-뇌 축만을 보았다고 하기 어렵고, 장-혈액-뇌 축을 완전히 배제하는 것이 불가능하다는 점과 동물이 인간과 다르다는 점이다. 따라서 장-신경-뇌 축을 재현한 인간 세포 유래 실험 모델(in vitro model)이 필요한 상태이다. 세포 실험을 위해서는 장과 뇌를 이어줄 수 있는 미주신경을 제작하는 것이 필요한데, 현재까지 내장 감각 신경을 세포 상태로 재현하는 방법이 밝혀지지 않았었다.
이에 서울대학교 묵인희 교수, 김종일 교수와 고려대학교 정석 교수 공동연구팀은 사람 역분화줄기세포(human induced-pluripotent stem cell, hiPSC)에서 내장 감각 신경 오가노이드(visceral sensory ganglion organoid, VSGO)를 유도하는 방법을 최초로 개발하였으며, 이를 생체 칩 내에 이식 후 사람 대장 오가노이드(human colon organoid, HCO)와 연결한 장-신경 축을 세포 실험 모델에서 구현하고, 알츠하이머병의 원인 병적 단백질인 아밀로이드/타우 단백이 VSGO로 전파될 수 있음을 입증하였다. 연구팀은 이러한 전파에 기존 알츠하이머 치매의 위험 유전자로 잘 알려진 APOE4 유전자형을 가지고 있으면 더욱 병적 단백질이 많이 전달되는 것을 확인하였으며, LRP1 이라는 단백질이 이러한 전파를 매개하는 것을 밝혀내었다.
이번 연구는 최초로 내장 감각 신경을 시험관 내에서 유도하는 방법을 확립하였다는 점과 내장 감각 신경이 알츠하이머 치매 발생의 단초가 될 수 있음을 밝혀내었다는 점에서 큰 의의가 있으며, 내장 감각 신경은 아밀로이드 베타나 타우와 같은 병적 단백질의 전파뿐만 아니라 이 신경을 통해 혈액-뇌 장벽을 우회하여 치료 약물을 전달하는 기술을 개발하는 데에도 큰 도움이 될 것이다.

Neddylation steers the fate of cellular receptors
Experimental & Molecular Medicine

(생리학교실, 교신저자)

(현 Harvard Medical School/
전 생리학교실, 제1저자)
세포 수용체는 막 수용체와 세포내 수용체로 구성되어 있으며, 리간드와 상호작용하여 생리적 반응을 조절하며 세포 간 소통에서 중요한 역할을 한다. 네딜화는 유비퀴틴과 유사한 아미노산 구조를 가진 NEDD8이라는 폴리펩타이드(polypeptide)가 표적 단백질에 공유결합 하는 것이다. 본 연구팀은 세포의 각 수용체 네딜화가 수용체의 안정성, 신호 전달 효율, 단백질 응집 및 전사 활성 등을 조절하는 방법에 대해 조사함으로써 수용체 네딜화에 의한 정형적, 비정형적 세포 생리 변화를 체계적으로 정리했다.