[연구동향]
Epigenetic scars in regulatory T cells are retained after successful treatment of chronic hepatitis C with direct-acting antivirals
Journal of Hepatology

(내과학교실,공동교신저자)

(보라매병원 소화기내과,
공동제1저자)
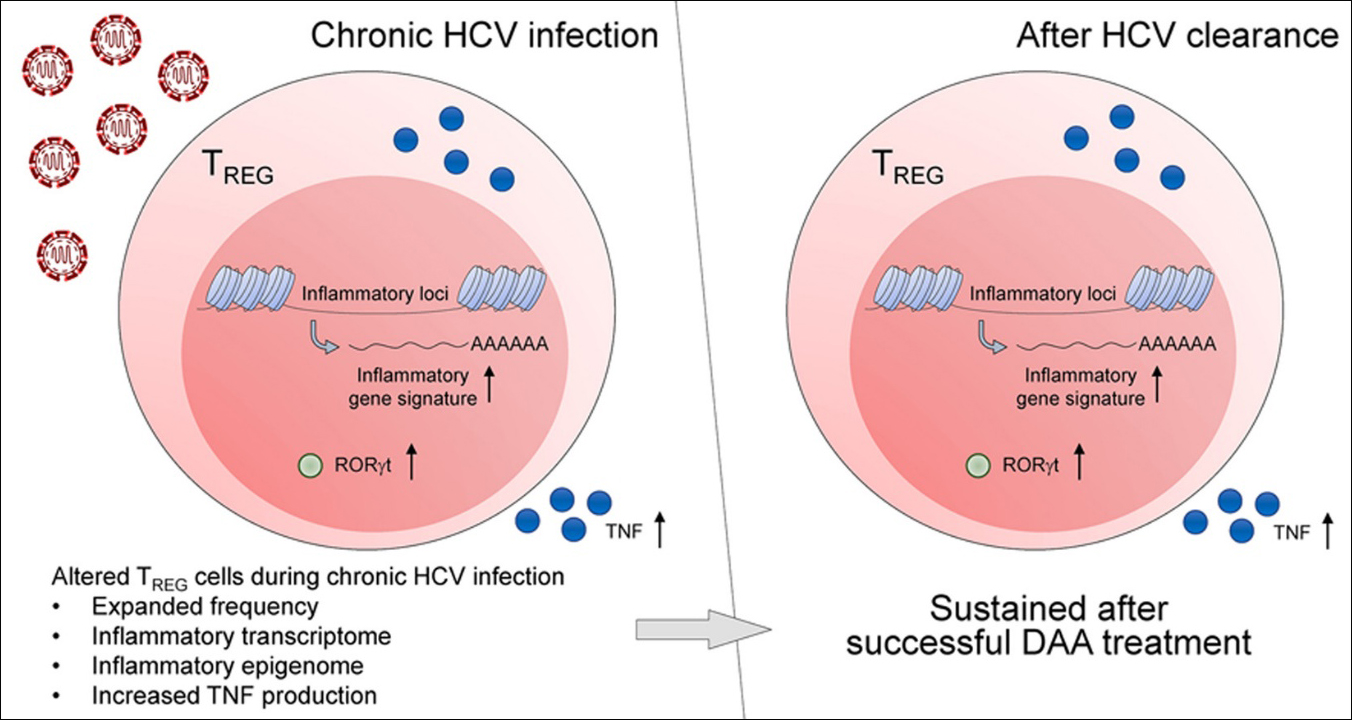
이 연구는 만성C형간염 환자의 조절 T 세포(TREG)에서 나타나는 변화를 직접작용 항바이러스제(DAA) 치료 전후로 조사했다. 연구 결과, 만성C형간염 환자의 말초혈액에서 조절 T 세포, 특히 활성화된 조절 T 세포의 비율이 증가했으며, 이러한 증가는 바이러스 제거 후에도 지속되었다. RNA-seq 분석 결과, 바이러스 제거 후에도 조절 T 세포의 염증성 특징(조절 T 세포 활성화, TNF 신호 등)이 지속되는 것으로 나타났으며, ATAC-seq 분석을 통해 조절 T 세포의 후성유전학적 변화가 치료 후에도 유지됨을 확인하였다.
이러한 발견은 세포 내 사이토카인 염색법으로 검증되었는데, 조절 T 세포의 염증성 특징과 TNF 생산이 만성C형간염 감염 중에 나타나고 바이러스 제거 후에도 지속됨을 보여주었다. 장기 추적 관찰 결과, 치료 완료 1년이 넘게 지난 후에도 이러한 변화가 부분적으로 유지되는 것으로 나타났다. 조절 T 세포의 전사체와 후성유전체 특성은 건강한 상태로 일부 정상화되는 경향을 보였지만, 여전히 일부 염증성 특징이 지속되었다.
이 연구 결과는 만성C형간염이 조절 T 세포에 장기적인 후성유전학적 반흔을 남기며, 이로 인해 바이러스 제거 후에도 염증성 특징이 지속될 수 있음을 시사한다. 이는 직접작용 항바이러스제 치료 후 면역 기능의 불완전한 회복을 설명하는 기전을 제시하며, 향후 치료 전략 수립에 중요한 통찰을 제공한다.
논문링크 : https://www.journal-of-hepatology.eu/article/S0168-8278(24)02317-1/abstract
The protective roles of integrin α4β7 and Amphiregulin-expressing innate lymphoid cells in lupus nephritis
Cellular & Molecular Immunology

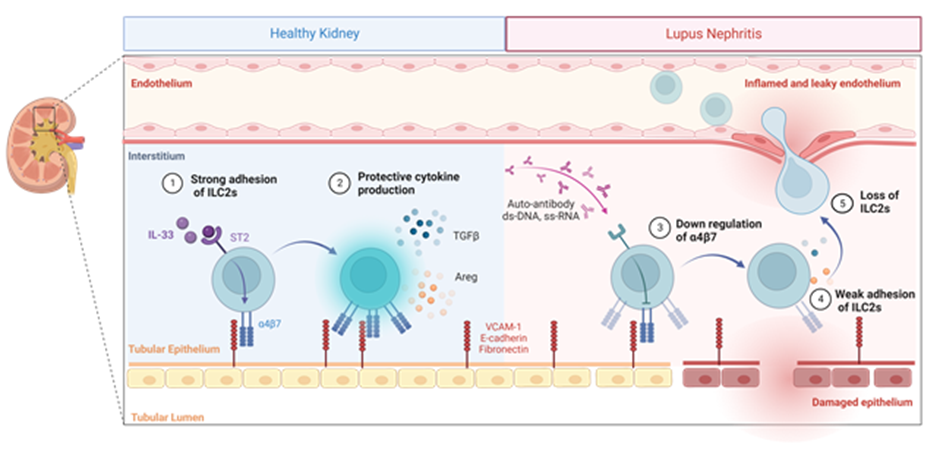
루푸스 신염은 전신성 홍반성 루푸스(SLE)에 의해 유발되는 심각한 신장 염증성 질환으로, 신장 기능의 손상과 만성 신부전으로 이어질 수 있다. 이번 연구는 루푸스 신염과 같은 신장 염증성 질환에서 ILC2(2형 선천성 림프구)의 접착과 이동 메커니즘을 조사하여, integrin α4β7이 신장에서 ILC2를 유지하고 기능을 발휘하는 데 중요한 역할을 한다는 것을 밝혀냈다. 연구 결과에 따르면, integrin α4β7은 VCAM-1, E-cadherin 또는 fibronectin과 결합하여 ILC2가 신장 내에 머무르도록 돕는다. 이때, integrin α4β7의 발현이 줄어들면 ILC2가 신장에 머무를 수 없게 되고 동시에 ILC2가 생산하는 복구성 사이토카인인 amphiregulin(Areg)의 생산도 감소하여 염증이 악화된다. 흥미롭게도, ILC2를 활성화시킬 수 있는 선천성사이토카인인 IL-33 처리는 ILC2에서 integrin α4β7과 Areg 발현을 증가시켜 질환이 유도된 마우스의 생존을 개선하고 루푸스 신염의 염증을 감소시키는 것으로 나타났다.
이 연구는 ILC2의 접착을 타겟으로 하는 새로운 치료 전략이 자가면역 신장 질환 치료에 유망할 수 있음을 시사하며, 이를 통해 자가면역 질환의 새로운 치료 가능성을 모색할 수 있을 것으로 기대된다.
Criteria for selecting living liver donors to optimize recipient outcomes in pure laparoscopic donor right hepatectomy: a cohort study
International Journal of Surgery

(외과학교실,교신저자)

(서울대학교병원 외과,제1저자)
최근 복강경 기술의 개발과 복강경 술기의 경험 축적으로 생체기증자 간이식에서 기증자 간 절제술도 점차 순수 복강경으로 시행하고 있다. 특히 기술적으로 제일 어렵다고 알려져 있는 우간절제술도 최근 서울대학교병원에서는 90% 순수 복강경으로 시행하고 있다. 이에 따라 기증자의 안전과 기증자측 인자 관련 연구 결과는 다수 보고하였으나 아직까지 수혜자 결과에 초점을 맞춘 기증자 선택 기준에 대한 연구는 없었다.
이 연구는 우선 순수 복강경 기증자 우간절제술(pure laparoscopic donor right hepatectomy, PLDRH)이 우선적으로 고려되어지는 요즘, PLDRH를 받는 기증자와 수혜자가 같은 기간 개복 기증자 우간 절제술(conventional open donor right hepatectomy, CDRH)을 받은 기증자와 수혜자와 어떤 특성이 다른지 살펴보았다. 개복 절제술을 시행한 기증자군의 연령이 더 많았고, 잔여 간 용적이 작았으며, 여러 개의 문맥 또는 담관 개구부가 예상되는 경우가 더 많았다.
특히, 고령의 기증자(40세 이상), 제한된 잔여 간 용적(35% 이상), 다수의 문맥 개구부가 예상되는 경우와 같은 특정 기증자 조건에서는 순수 복강경을 이용한 경우보다 통상적인 개복 우간절제술을 시행한 군에서 수혜자 조기 주요 합병증률이 적었다. 즉, 이와 같은 특정 조건을 가진 기증자에서는 개복 우간절제술을 우선적으로 고려하는 것이 필요할 수 있음을 밝혔다.
생체기증자 간이식은 간기증자의 안전을 최우선으로 생각해야함이 맞지만 동시에 수혜자의 수술 결과 또한 중요함을 잊지 말아야 하며, 술기를 결정함에 있어서 이번 결과를 바탕으로 의료진간, 그리고 환자, 보호자와 충분한 상의 하에 결정하는 것이 필요함을 보여 준다.

Tislelizumab plus chemotherapy versus placebo plus chemotherapy as first line treatment for advanced gastric or gastro-oesophageal junction adenocarcinoma: RATIONALE-305 randomised, double blind, phase 3 trial
British Medical Journal

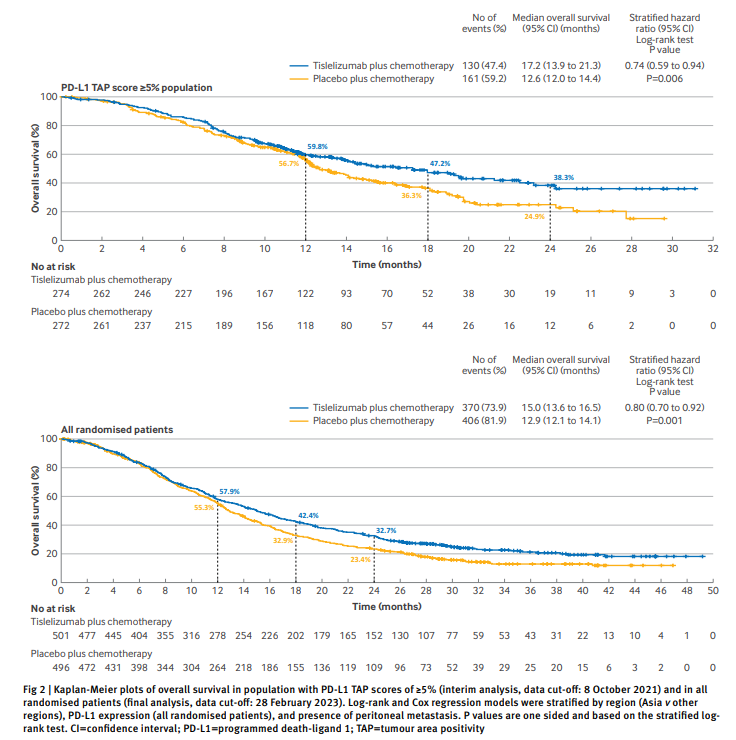
진행성, 전이성 위암, 그 중에서 특히 HER2 음성 위암에서 세포독성항암치료는 오랫동안 전세계표준치료로 사용되어 왔다. 이 환자들의 전체 생존기간의 향상을 위해 새로운 약제를 이용한 다양한 임상연구들이 진행되고 있다. 본 RATIONALE-305 임상연구는, 면역항암제를 기존의 표준 세포독성항암치료에 추가하였을 때, 생존기간의 향상을 이룰 수 있는지를 보고자 계획된 연구이다. 아시아, 유럽, 북미를 포함한 전 세계의 146개 기관에서 진행된 전세계적 연구이고, 무작위 배정, 3상 임상연구이다. 이 연구에서는 면역항암제 Tislelizumab을 사용하였고, 이 약제는 nivolumab(옵디보)이나 pembrolizumab(키투르다)과 같은 작용기전을 가진 PD-1 억제제인 면역관문 억제제이다. 전 세계에서 1657명의 환자가 등록되었고, 최종적으로 997명의 환자가 항암치료+위약군(496명)과 항암치료+Tislelizumab(501명)으로 각각 무작위 배정되었다. Tislelizumab 군이 위약군에 비해 의미 있는 생존기간의 향상을 보였다. 전체 무작위 배정된 환자에서는 중앙생존기간이 15개월(Tislelizumab 군) 대비 12.9개월(위약군)로, 위험비 0.8을 보여 주어서 사망위험도를 20% 감소시켰고, 이는 통계적으로도 의미 있는 수치였다. 특히 암조직에서의 PDL1 TAP 수치가 5%이상인 환자군에서는 중앙생존기간이 17.2개월(Tislelizumab 군) 대비 12.6개월(위약군)로, 위험비 0.74를 보여 주어서 사망위험도를 26% 감소시키는 결과를 보여 주었다. 전체 환자군과 PDL1 TAP 5%이상인 환자군 모두에서 생존기간의 유의미한 호전을 보여 주어, 이 RATIONALE-305 3상연구는 성공적인 연구로 선언되었다. 부작용 측면에서도, 3등급 이상의 치료관련 이상반응이 Tislelizumab 군에서는 54%의 환자에서, 위약군에서는 50%의 환자에서 보고되어서 큰 차이가 없었고, 대부분의 이상반응은 잘 관리가 되는 이상반응이었다. 이 연구는 특히, 전세계적으로 진행된 3상연구이지만, 전세계적으로 위암환자의 분포가 아시아에 좀 더 많은데, 이러한 환자 발생 역학을 잘 반영하여, 전체 등록된 환자군에서 아시아 환자가 비아시아 환자에 비해 좀 더 많은 분포를 가지고 있어서, 현실 세계의 위암환자를 잘 반영하여 진행된 연구라는 점에서도 큰 의의가 있다.
Immunogenicity, reactogenicity, and safety of two-dose adjuvanted herpes zoster subunit vaccine in patients with systemic lupus erythematosus in South Korea: a single-centre, randomised, double-blind, placebo-controlled trial
The Lancet Rheumatology

(내과학교실,교신저자)

(내과학교실,공동 제1저자)

(분자의학 및 바이오제약학과,
공동 제1저자)
일반인을 대상으로 한 기존 연구에서는 대상포진 subunit 백신의 효능과 안전성이 입증되었으나, 면역체계의 이상 및 각종 면역억제제의 복용으로 인해 면역력이 저하된 전신 홍반 루푸스(systemic lupus erythematosus, SLE) 환자에게도 동일한 효과를 발휘하는지에 대한 연구는 부족했다. SLE 환자를 대상으로 한 무작위 배정, 이중맹검, 위약 대조 임상시험에서 대상포진 subunit 백신의 면역원성, 반응원성 및 안전성을 규명하는 것을 목표로 하였다.
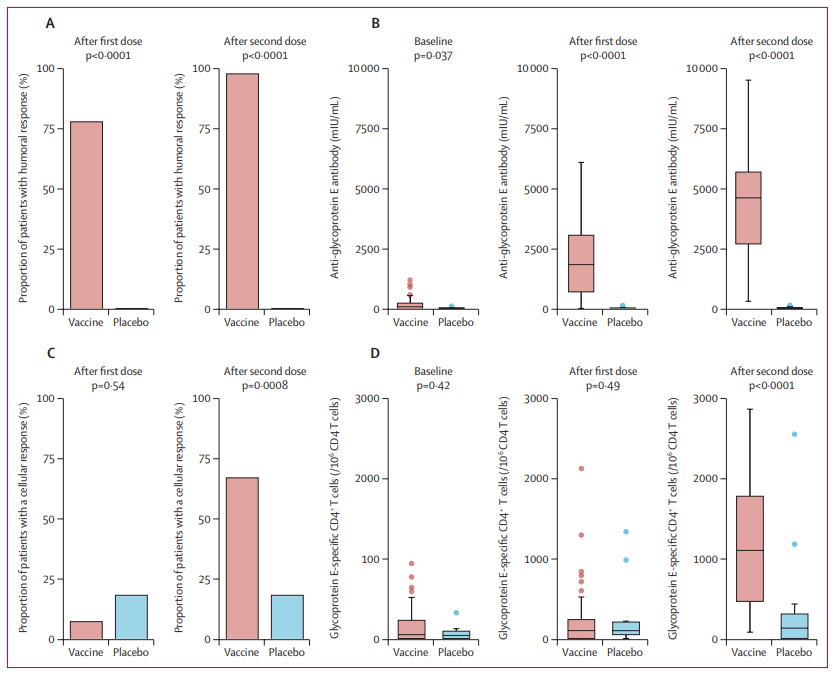
본 연구에서는 루푸스 환자 60명을 무작위로 배정하여 49명에게는 대상포진 subunit 백신을, 11명에게는 대조약을 2회 접종하였다. 2차 접종 4주 후 백신에 대한 항체(체액 면역) 반응과 세포 면역 반응을 평가하였다. 백신 접종군에서는 98%, 대조군에서는 0%의 항체 반응이 관찰되었다. 세포 면역 반응 또한 대조군에 비해 백신 접종군에서 더 높았지만, 건강인을 대상으로 진행된 이전 연구 결과에 비해서는 낮았다. 백신군에서 주사 부위 반응, 발열, 피로가 더 많이 보고되었으나 중대한 부작용은 없었다. 또한, SLE 질병 활성도 및 재발률에서는 두 그룹 간 차이가 없었다.
본 연구는 루푸스 환자에서도 대상포진 subunit 백신이 면역 반응을 유도하며 안전하게 사용될 수 있음을 입증하였다는 점에서 의의가 있다. 그러나 체액 면역 반응과 달리 세포 면역 반응은 건강인보다 낮은 수준이어서, 향후 이 부분에 대한 추가 연구가 필요하다.
논문링크 : https://www.thelancet.com/journals/lanrhe/article/PIIS2665-9913(24)00084-5/fulltext
Improvement in health-related quality of life following antibiotic treatment in nontuberculous mycobacterial pulmonary disease: Initial analysis of the NTM-KOREA cohort
Clinical Infectious Diseases

(내과학교실,교신저자)

(서울대학교병원 내과,제1저자)
비결핵항산균 폐질환은 결핵을 제외한 마이코박테리아에 의한 폐 감염증을 일컫는데, 지난 10년 사이에 국내에서만 발병률이 3배 이상 증가하였으며, 최근에는 발병 건수 측면에서 결핵을 앞지르기 시작하였다. 이러한 역학적 중요성에도 불구하고, 비결핵항산균 폐질환의 항생제 치료 성공률은 30~60%에 불과한 실정이다. 이에 최근에는 항생제 치료를 통해 미생물학적 완치 외에도, 환자의 삶의 질을 개선시키는 것을 주요 목표로 하는 움직임이 있다.
서울대학교 연구진은 국내 8개의 지역 거점 병원 및 1개의 중앙연구소가 참여하는, NTM-KOREA 프로젝트를 이끌고 있다. NTM-KOREA는 비결핵항산균 폐질환에 대한 치료를 받는 환자를 전향적으로 추적하면서, 미생물학적 치료 반응뿐 아니라 삶의 질, 운동 능력, 식이 섭취 등의 변화를 10년에 걸쳐 추적하는 대규모 프로젝트이다.
이번 연구에서는 2022년 2월부터 2023년 8월 사이에 NTM-KOREA에 참여한 411명 환자의 삶의 질을 분석하여 발표하였다. 치료 시점부터 6개월 단위로 “QOL-B”라고 하는 설문지를 통해 삶의 질을 추적하였다. QOL-B는 신체 기능 및 호흡기 증상을 포함한 8개의 영역에 걸쳐 삶의 질을 측정하는데, 점수가 높을수록 삶의 질 역시 좋음을 의미한다. 이번 연구에서는 항생제 치료 6개월 이후 31.1%의 환자에서 호흡기 증상이 유의하게 호전되었는데, 이러한 호전은 미생물학적 반응과는 관련이 없었다. 한편, 26.8%의 환자가 단기간의 치료를 통해 신체 기능의 유의미한 개선을 경험하였고 이 역시 미생물학적 치료 반응과는 관련이 없었다.
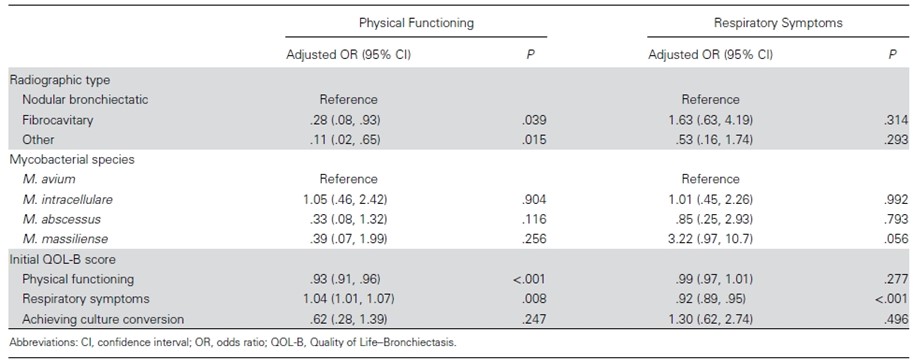
환자들이 경험하는 삶의 질 개선, 특히 신체 기능과 호흡기 증상의 개선은 치료 시작 시점의 신체 기능이 떨어진 경우, 그리고 호흡기 증상이 심한 경우에 더욱 뚜렷하였다. 초기 신체 기능(adjusted odds ratio 0.93, 95% CI 0.91-0.96) 및 호흡기 증상(adjusted odds ratio 0.92, 95% CI 0.89-0.95)의 점수가 높을수록 항생제 치료를 통해 이러한 영역이 개선될 가능성은 낮아졌는데, 이는 “초기 신체 기능이 떨어지거나 호흡기 증상이 심한 환자일수록 치료를 통해 개선될 여지가 더 큼”을 의미한다. 마찬가지로 이러한 개선은 미생물학적 치료 반응과 관련이 없었다.
이 연구의 결과는, 초기 중증도가 심한 환자일수록 미생물학적 치료 반응과 관계없이 삶의 질 개선 가능성이 크므로 더욱 적극적인 항생제 치료가 필요함을 시사한다.
논문링크 : https://academic.oup.com/cid/article/78/6/1690/7638908?login=true

