[연구동향]
Genome-wide association study identifies novel susceptibilities to adult moyamoya disease
Journal of Human Genetics, 2023

(신경외과학교실,교신저자)

(한림대학교 의과대학,제1저자)
서울대학교 의과대학 신경외과학교실의 김정은 교수팀 (김정은, 조원상, 이성호, 강현승, 김강민, 하은진 교수)은 한림대학교 의과대학 신경외과학교실의 전진평 교수와 함께 전장유전체상관분석으로 희귀난치질환인 성인 모야모야병에서 감수성 유전자로 기존에 알려진 RNF 213 외에 17번 염색체에서 가능성이 있는 감수성 유전자의 후보군을 찾아내었다. 2011년 일본 교토대학교 연구팀과의 협력연구로 세계 최초로 모야모야병의 감수성 유전자로 RNF213을 발견하여 발표했던 연구팀은 이후 한국인 환자를 대상으로 한 전장유전체상관분석을 통해 RNF213 외에 감수성유전자의 후보군을 찾아내어 발표하였고, 이는 한국인 성인 모야모야병의 유전적 소인 및 임상경과 등과 연관하여 획기적인 발견으로 향후 모야모야병의 예후 예측 및 치료의 발전에 도움이 될 수 있는 연구로 평가가 된다. 특히 서울대학교 신경외과학교실 팀은 최근 발표된 세계 모야모야병 연구동향을 보고한 논문에서도 중국 수도의과대학에 이어 세계 2위의 업적으로 평가받았던 바 있다.
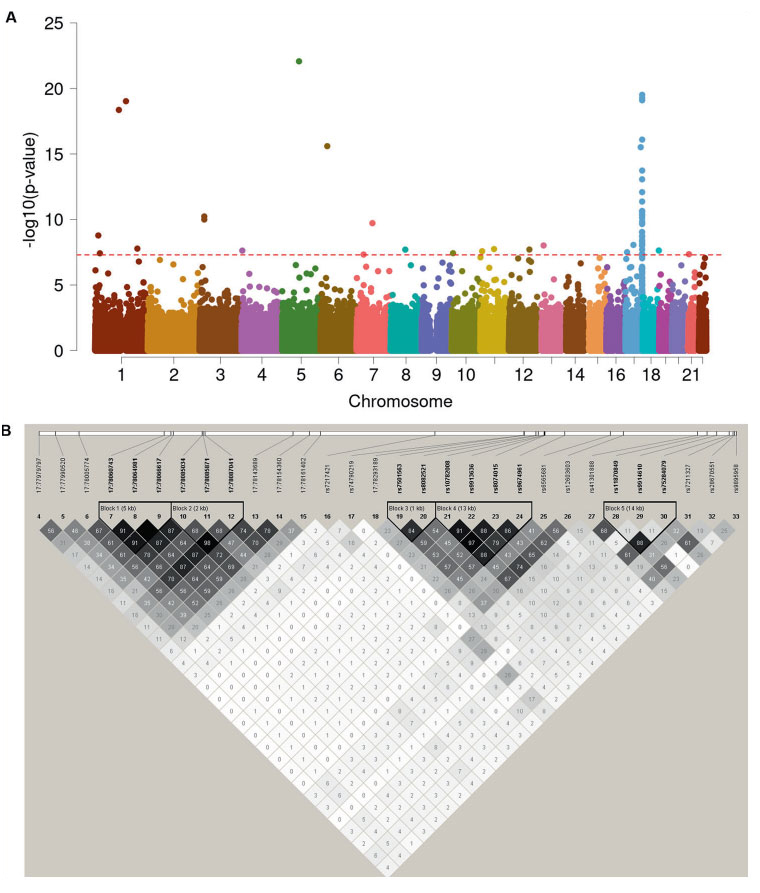
A Manhattan plot of genome-wide association study involving adult moyamoya disease after adjusting for age, gender, hypertension, diabetes mellitus, hyperlipidemia, and smoking, and four principal components. X- and Y-axes represent chromosome number and –log10 transformed p-value, respectively. Red sub-line indicates a genome-wide significance threshold (P = 5 × 10−8). B A plot of linkage disequilibrium (LD) blocks in 17q25.3 region composed of genome-wide significant associations (i.e., 30 SNPs). Five LD blocks showing strong LD (r2 > 0.8) include: 17:78060743 with 17:78064981 and 17:78066617 (CCDC40, r2 = 0.91); 17:78085034 with 17:78085034 (GAA, r2 = 0.98); rs8082521 with rs7501563 (RNF213, r2 = 0.84); rs10782008 with rs9913636, rs8074015, and rs9674961 (RNF213, r2 = 0.91, 0.97, and 0.88, respectively); and rs11870849 and rs75284079 (ENDOV, r2 = 0.88). The colored areas in each block indicate R-square (R2) values
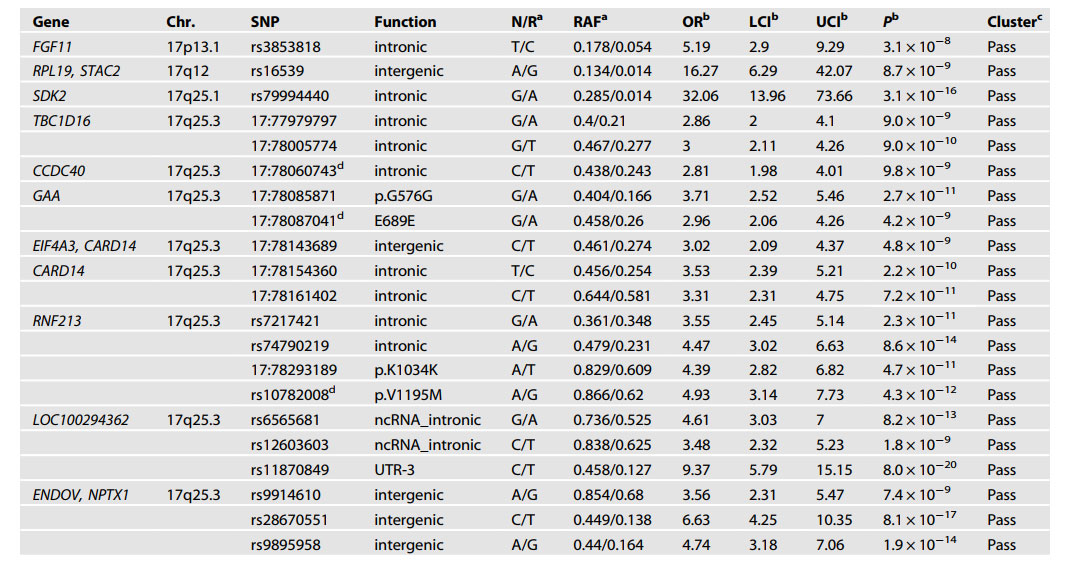
aN/R indicates non-risk and risk allele; Risk allele frequency (RAF) shows cases in left and controls in right
bOdds ratio (OR), lower/upper 95% confidence interval (LCI and UCI), and P values were estimated under the multivariate logistic regression model after adjustment for age, gender, hypertension, diabetes mellitus, hyperlipidemia, and smoking, and four genetic ancestr y values
cEvaluation of genotype cluster distribution of each SNP shown genome-wide significance threshold through scanning the PolyHighResolution under the Axiom™ Genotyping Solution Data Analysis (Pass, well-clustered; Hold, ambiguous clustered; Fail, bad-clustered)
dOne SNP was listed due to a strong linkage disequilibrium (LD, r2 > 0.8): 17:78060743 with 17:78064981 and 17:78066617 (CCDC40, r2 = 0.91); 17:78085034 with 17:78085034 (GAA, r2 = 0.98); rs8082521 with rs7501563 (RNF213, r2 = 0.84); rs10782008 with rs9913636, rs8074015, and rs9674961 (RNF213, r2 = 0.91, 0.97, and 0.88, respectively); and rs11870849 and rs75284079 (ENDOV, r2 = 0.88)
Measures of connectivity and dorsolateral prefrontal cortex volumes and depressive symptoms following treatment with selective serotonin reuptake inhibitors in adolescents
JAMA Network Open, 2023

(정신과학교실,교신저자)

(서울대학교병원 소아정신과,
제1저자)
청소년 우울증의 치료에는 항우울제가 널리 사용되며, 특히 중등도 이상의 우울증 청소년의 1차 약물 치료로는 선택적 세로토닌 재흡수 차단제(Selective Serotonin Reuptake Inhibitor: SSRI)를 처방한다. 다만 SSRI는 단일 제제 사용 시의 관해율이 55%, 인지 행동 요법 등의 다른 치료와 병행 시 관해율이 60% 정도로, 청소년 우울증의 치료 효능을 더욱 향상시킬 필요가 있다. 이를 위해서는 우울 증상 호전과 관련된 신경생물학적 변화를 이해하고 치료 지표를 규명하는 것이 중요하다. 하지만 청소년 우울증의 신경생물학적 치료 기전에 대한 연구는 전세계적으로 아직 미흡한 실정이다.
연구진은 서울대학교어린이병원 소아청소년정신과 Mood and Anxiety of Youth (MAY) 클리닉에 내원한 우울증 청소년 95명과 우울증이 없는 청소년 57명을 대상으로 연구를 수행했다. 우울증 청소년은 SSRI 계통의 항우울제인 에스시탈로프람(escitalopram)으로 8주간 치료했다. 치료 전과 후, 소아청소년 우울증 평가 도구인 Children’s Depression Rating Scale-Revised (CDRS-R)로 우울 증상을 평가했고, 해부학적 뇌 자기공명영상(MRI)과 휴지기 기능적 자기공명영상(resting-state fMRI) 데이터를 수집했다. 치료 전에 비해, 치료 후 우울 증상이 40% 이상 감소한 청소년을 치료반응군으로, 그렇지 않은 군을 치료비반응군으로 분류했고, 치료 전후의 우울 증상 변화와 뇌 구조 및 휴지기 기능적 연결성(resting-state functional connectivity)의 변화를 분석했다. 특히 연구진은 정서 조절과 인지 통제에 관여하는 주요 뇌 영역인 배외측 전전두피질의 부피와 휴지기 기능적 연결성의 변화가 우울 증상의 변화와 관련이 있는지를 분석했다.
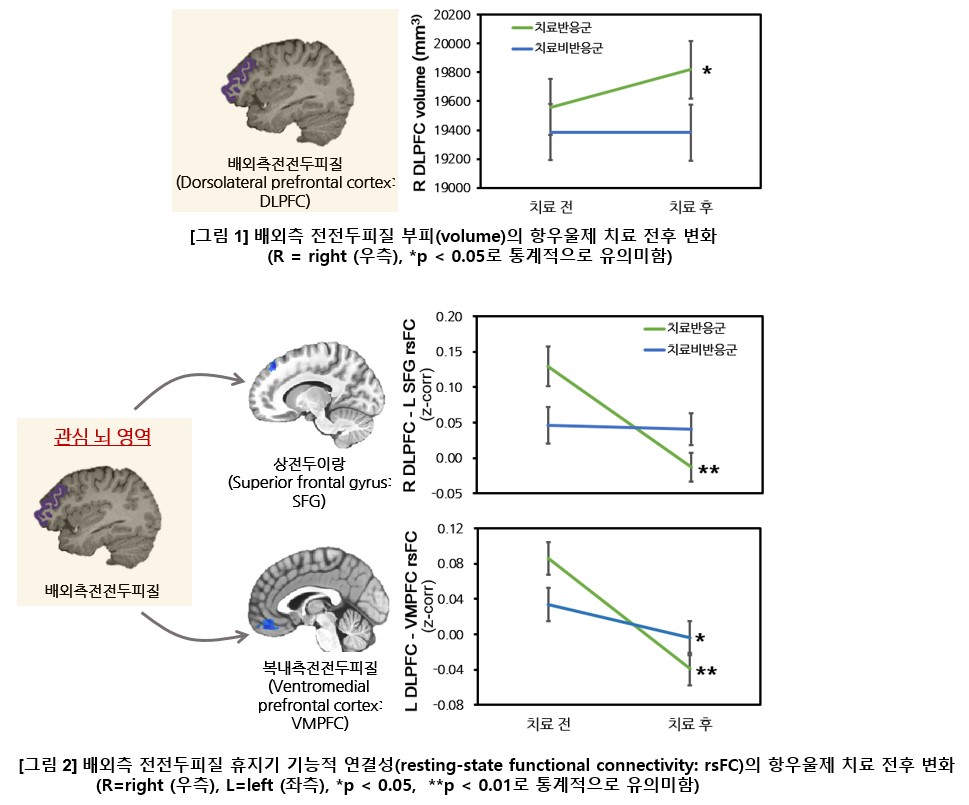
우울증 청소년의 54%가 항우울제 치료 후 우울 증상이 개선된 치료반응군으로 분류되었다. 항우울제 치료 후, 치료비반응군에 비해 치료반응군에서 배외측 전전두피질의 부피가 증가했고(그림 1), 배외측 전전두피질과 상전두이랑(superior frontal gyrus) 및 복내측 전전두피질(ventromedial prefrontal cortex) 사이의 기능적 연결성이 감소했다(그림 2). 또한 우울 증상이 더 많이 호전될수록 배외측 전전두피질 부피가 더 많이 증가했으며, 기능적 연결성은 더 많이 감소했다.
우울증에서 나타나는 전전두피질 부피의 감소는 신경 위축과 관련 있다고 알려져 있다. 항우울제 치료 후 배외측 전전두피질 부피의 증가는 우울증으로 인해 위축되었던 신경 세포의 회복과 관련 있을 가능성이 있다. 한편 휴지기는 정서나 인지 기능의 통제가 활성화되지 않는 뇌의 휴식 상태를 의미하는데, 치료 후 배외측 전전두피질의 휴지기 기능적 연결성이 감소한 것은 우울증 청소년이 치료 후 보다 편안한 뇌 연결 상태를 보이는 것으로 해석할 수 있다.
김재원 교수는 “항우울제 치료가 청소년 우울증에서 정서 조절 및 인지 통제를 담당하는 뇌 구조 및 기능적 연결성의 변화를 동반할 수 있다는 것을 보여준 연구 결과로, 뇌 구조 및 기능적 연결성의 변화는 항우울제 치료의 바이오마커로 활용될 수 있다”고 말했다.
논문링크 : https://jamanetwork.com/journals/jamanetworkopen/fullarticle/2808079
A single-cell atlas of in vitro multiculture systems uncovers the in vivo lineage trajectory and cell state in the human lung
Experimental & Molecular Medicine, 2023

(생화학교실,공동교신저자)

(병리학교실,공동교신저자)

(케임브리지대학교,공동교신저자)

(의과학과,공동제1저자)

(의과학과,공동제1저자)

(의학과,공동제1저자)
서울대학교 의과대학 유전체의학연구소 김종일 교수 (제1저자 이우찬 박사, 이세윤 박사과정, 윤정기 박사), 영국 케임브리지 대학교 이주현 교수, 분당서울대학교병원 정진행 교수 공동연구팀이 2023년 인체 유래 폐 기도 오가노이드(Lung Airway Organoid)를 활용한 단일세포전사체 분석을 통해 최근 각광받고 있는 오가노이드의 줄기세포 분화도 연구와 질병 모델로서의 가능성을 확인한 연구 결과를 발표했다.
동물실험의 대안으로 각광받고 있는 오가노이드 기술은 인체 줄기세포 및 장기 기원세포를 실험실 환경에서 3D 배양법을 활용해 만드는 미니 장기이다. 현재 장기별로 다양한 배양조건이 새롭게 발표되고 있고 오가노이드의 장기 줄기세포 연구, 질병기전 연구 모델, 기증자별 맞춤의학 연구 등 다양한 활용도가 기대되어 빠르게 발전 중인 연구기법이다.
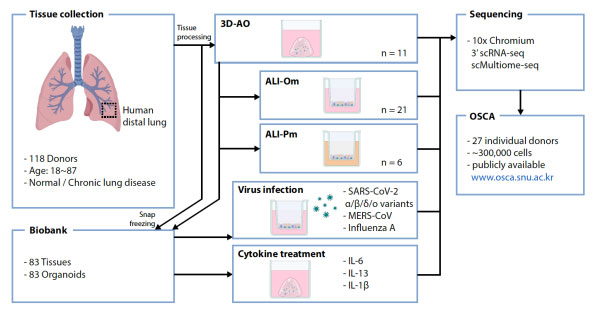
본 연구진은 총 27명의 기증자로부터 장기 기원세포를 분리해내 성체줄기세포 유래 폐 기도 오가노이드를 제작하여 배양조건별 분화도 평가, 기증자 개인차 분석, 실제 조직과 오가노이드의 차이, COVID-19 바이러스를 이용한 감염질환 모델 평가까지 조건별로 유전자적 특성을 확인하기 위해 단일세포전사체 분석을 시행하여 폐 오가노이드 단일세포지도를 제작하여 공개하였다.
그 결과, 3D 배양조건으로 키워진 폐 기도 오가노이드가 기존 폐 상피 세포 연구에 많이 사용되었던 2D ALI(Air-Liquid Interface) 배양법과 유사한 수준의 상피세포 분화도를 보이는 것으로 확인되었다. 줄기세포로 알려진 기저세포(Basal)부터 곤봉체 세포(Club), 배상 세포(Goblet), 섬모 세포(Ciliated)가 두 가지 배양 조건에 모두 존재함을 확인했다.
특히, 실제 조직내에서 극히 적은 비율로 존재해 희귀세포로 분류되는 ionocyte, pulmonary neuroendocrine, tuft cell까지 모두 두 가지 배양 조건에서 존재했고, 분화도 분석을 통해 줄기세포로부터 희귀세포들까지의 분화 중간단계 세포의 전사체 분석 또한 가능했다. 희귀세포는 그 비율은 적지만 인체내에서 항상성 유지에 중요한 역할을 하는 것으로 알려져 있기에, 해당 세포들의 분화도 연구는 추후 분화 유도 방법 개발 등 여러 활용성이 있을 것으로 평가된다.
본 연구진은 수립된 오가노이드를 COVID-19 바이러스를 비롯한 다양한 호흡기 바이러스 감염 모델로 활용했다. COVID-19 바이러스 다양한 변종들을 포함하여, 인플루엔자 바이러스, 메르스 코로나 바이러스까지 오가노이드에 감염시켜 단일세포 전사체 분석을 진행하였다. 그 결과, 폐 기도 오가노이드 세포에는 인플루엔자 바이러스에서 가장 높은 감염률을 보인 것을 확인했다.
본 연구결과로 구축된 데이터베이스(OSCA, osca.snu.ac.kr)는 폐 기도 오가노이드를 활용하는 국내외 연구진들에게 공개되어 그 활용성 평가 및 특성 분석에 중요하게 사용될 것으로 여겨진다. 이번 연구는 우리나라를 대표하는 의생명과학 저널인 ‘Experimental & Molecular Medicine’ (IF=12.8) 최신호에 출간됐다 (논문명: A single cell atlas of in vitro multi-systems uncovers in vivo lineage trajectory and cell state in the human lung).
이번 연구는 한국연구재단을 통해 지원된 과학기술분야 기초연구사업 과제 중, 과학기술정보통신부의 재원으로 수행된 중견연구사업과, 교육부의 재원으로 수행된 대학중점연구소의 지원으로 이루어졌으며, 교육부 주관의 기초과학연구역량강화 사업을 통해 선정된 유전체의학핵심연구지원센터의 장비를 활용하여 수행되었다.
A new era of macrophage-based cell therapy
Experimental & Molecular Medicine, 2023

(미생물학교실,교신저자)

(서울대학교병원 융합의학과,
제1저자)
최근 HER2 positive breast cancer 환자를 대상으로 chimeric antigen receptor-macrophage therapy (CAR-M)가 미국에서 임상 1상 시험에 들어가면서 마크로파지 세포치료제에 대한 관심이 증가하였다. CAR-M은 CAR-T와는 다르게 고형암에 대한 침투력이 높고 암세포에 대한 직접적인 탐식 및 제거능력을 보유하고 있어 뛰어난 면역항암치료제 후보로 기대감을 모으고 있다.
마크로파지를 세포치료제로 개발하고자 하는 노력은 종양에서뿐만 아니라 다양한 재생결핍성 난치성 질환에서도 이미 시도되어오고 있다. 임상 3상 시험으로 Anal fistula, osteonecrosis, limb ischemia가 적응증에 올라있고, 현재 MACI라는 autologous chondrocyte를 무릎연골재생 치료제로 판매하고 있는 Vericel에서는 dilated cardiomyopathy 환자를 대상으로 Ixmyelocel-T라는 마크로파지 세포치료제 임상 2상 시험을 진행 중에 있다. Vericel사는 마크로파지가 항염성과 혈관재생능력을 가지고 있어 손상된 조직을 재건하는 데에 뛰어난 효과를 보인다고 설명한다. 또한 2019년 영국 에딘버러 대학에서는 자가유래 마크로파지에 대한 간경화 임상 1상 시험을 성공적으로 진행한 바가 있다.
마크로파지는 환자의 혈액과 골수로부터 쉽게 분화가 가능하여 autologous cell source에 대한 접근이 쉽고, 제대혈의 혈액줄기세포에 대한 체외 증식과 분화를 통하여 allogenic cell source에 대한 접근도 비교적 쉬운 편이어서 세포치료제로서의 기본 조건을 갖추고 있다. 더불어 면역세포로서 목적 장기로의 유주에 능하고 내재적으로 조직의 리모델링과 항염유발을 위한 사이토카인을 분비하는 등 재생을 위한 전반적인 자체 기전을 가진다. 일반적인 resident macrophage의 수명이 일 년 이상인 것을 고려할 때 치료적 목적으로 주입한 마크로파지가 오랜 생존을 보일 것 또한 예측할 수 있다.
그러나 주위 환경에 민감하게 반응하여 자신의 표현형을 쉽게 바꾸는 마크로파지의 특성상 염증 환경에 투입한 마크로파지가 염증성 표현형을 획득하여 염증을 악화시킬 가능성이 있기 때문에, 세포치료제로 개발될 마크로파지는 안전성에 대한 주의 깊은 검증이 필요하다.
이를 극복할 수 있는 한 가지 방안은 염증성 표현형 획득에 필요적인 유전자를 CRISPR/CAS9 system을 통하여 변이를 일으키는 것으로, 본 연구진은 높은 효율로 염증성 유전자를 제거하고 안전한 사람 마크로파지 세포치료제를 획득하는 기술을 확립한 바 있다. 또한 유전자 조작 조직재생성 마크로파지의 조직재생효과를 전임상 모델에서 검증하였고, 이를 기반으로 차세대 재생촉진용 세포치료제 개발을 제안하였다.

Mass-produced gram-negative bacterial outer membrane vesicles activate cancer antigen-specific stem-like CD8+ T cells which enables an effective combination immunotherapy with anti-PD-1
Journal of Extracellular Vesicles, 2023

(의과학과/해부학교실,교신저자)

(의과학과,제1저자)
본 연구는 서울대학교 의과대학 의과학과/해부학교실 연구팀과 포항공과대학교 생명공학과 고용송 교수 연구팀이 공동으로 수행한 연구로, Metal precipitation과 size-exclusion chromatography를 결합한 새로운 제조 공정 방식을 개발하여 대장균으로부터 엑소좀(세포밖소포체)을 대량으로 분리 및 정제하고 이를 활용하여 여러 마우스 항암 모델의 완전 관해 및 종양미세환경 내 암 항원 특이적인 stem-like T 세포의 침투 및 활성화를 검증한 연구이다.
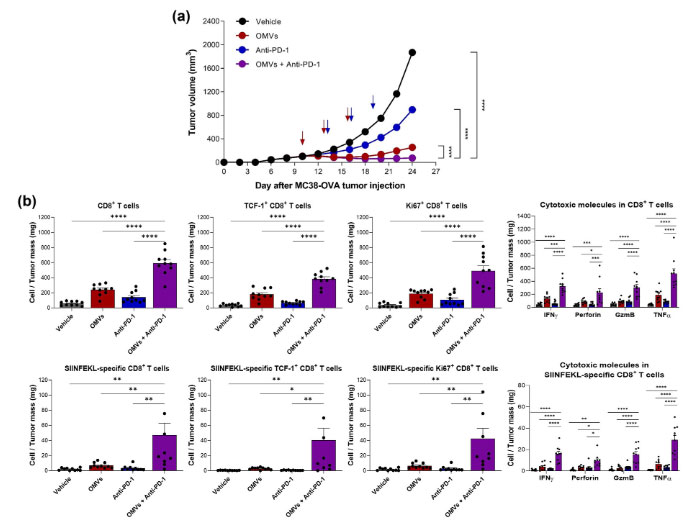
Gram-negative 및 Gram-positive 박테리아에서 유래된 세포밖소포체(EVs)가 뛰어난 항암 반응을 유도할 수 있음에도 불구하고, 박테리아 EVs의 대규모 생산은 새로운 면역항암치료제 개발의 장애물로 남아 있다. 본 연구에서는 Escherichia coli EVs, 즉 outer membrane vesicles (OMVs)의 대량 생산을 위한 새로운 제조 공정 방식을 개발하였다. Metal precipitation과 size-exclusion chromatography를 결합함으로써 160 L의 conditioned medium으로부터 3.93 × 1015 particles에 해당하는 357 mg의 E. coli OMVs를 분리하였다. 대량으로 생산된 E. coli OMVs를 활용하여 항암 반응을 확인한 결과, 두 개의 마우스 종양 모델의 완전관해가 유도되었고, 신항원을 발현하는 종양 모델에서 종양 미세환경에 대한 분석을 진행한 결과, E. coli OMVs에 의하여 CD8+ T 세포, 특히 TCF-1과 PD-1을 높게 발현하는 암 항원 특이 CD8+ T 세포의 침투와 활성화가 증가되는 것을 밝혀냈다. 또한 면역관문억제제로 널리 사용되고 있는 anti-PD-1 항체와의 병용투여를 진행하여 종양 성장 억제와 종양 미세환경 내 암 항원 특이적 stem-like CD8+ T 세포의 침투 및 활성화를 확인함으로 병용투여에 의한 시너지 효과를 검증하였다. 따라서 본 연구는 차세대 면역항암치료제 개발의 새로운 후보로서 E. coli OMVs의 뛰어난 항암 효과를 밝히고, 더 나아가 공정개발의 단계에서 매우 중요한 대량 생산 과정의 새로운 방법을 제시함에 있어 큰 의의가 있다.
논문링크 : https://onlinelibrary.wiley.com/doi/full/10.1002/jev2.12357
Development and validation of a reinforcement learning model for ventilation control during emergence from general anesthesia
npj Digital Medicine, 2023

(마취통증의학교실,교신저자)

(서울대학교병원 마취통증의학과,
공동제1저자)

(마취통증의학교실,
공동제1저자)
본 연구는 마취에서 회복 중인 환자에서 인공 호흡기를 제어하기 위한 인공지능 알고리즘을 개발하고 이를 외부 검증한 다기관 코호트 연구로 본교 이형철 교수, 윤현규 교수와 서울대학교병원 이현훈 교수, 박지수 교수, 분당서울대학교병원 구창훈 교수, 보라매병원 원동욱 교수 등이 참여하였다.
일반적으로 마취에서 깨어나는 동안 환자의 충분한 자발 호흡이 회복될 때까지 의사는 심폐 불안정성 없이 인공 호흡을 지원해야 한다. 우리 연구실은 자체 개발한 Vital Recorder를 이용해 2016년부터 마취 중 인공호흡기 및 활력 징후 데이터를 수집해 오고 있다. 현재 이 프로그램은 국내 30개 이상의 병원에 적용되어 활용되고 있고, 이러한 통일된 형식의 데이터는 전세계에 유래가 없는 것이기 때문에 본 연구가 가능하였다.
이 데이터를 이용해 우리는 우선 전신 마취에서 회복 중 인공호흡을 제어하기 위한 강화 학습 기반 인공호흡 모델(AIVE)을 개발하고 이를 외부 검증하였다. 2016년부터 2019년까지 서울대학교병원에서 진행된 14,306건의 수술 사례에서 얻은 환기 및 혈역학 파라미터가 모델 학습 및 내부 테스트에 사용되었다. 2022년에는 분당서울대학교병원의 406건의 사례를 포함하는 외부 검증 코호트의 데이터는 모델 성능을 평가하는데 사용되었다.
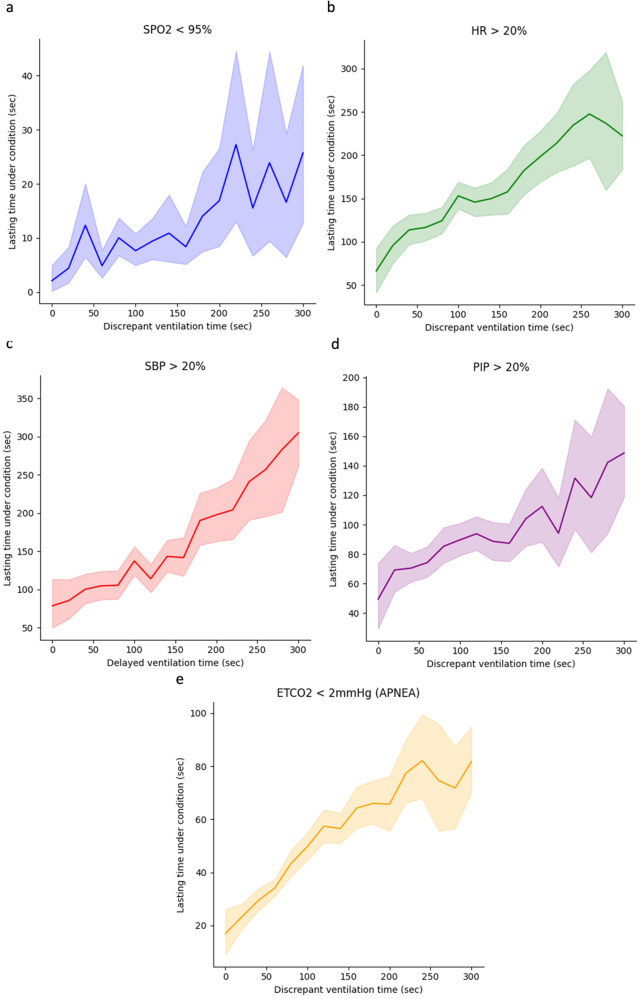
강화학습 모델을 개발할 때는 보상(reward)을 어떻게 정의하느냐가 중요하다. 우리는 모델의 보상을 97% 이하의 산소포화도, 6초 이상의 무호흡, 그리고 20% 이상의 심박수, 수축기 혈압, 기도압력 상승으로 정의하였다.
학습된 모델의 성능은 내부 검증 및 외부 검증에서 임상의 정책보다 높은 보상을 취득했다. 이로부터 모델이 최소한 잘 학습되었다는 것을 확인할 수 있다. 실제 임상적 성능을 평가한 결과에서, 임상의의 인공호흡이 모델의 인공호흡과 일치할수록 심폐 불안정성이 최소화되었다.(95% 이하의 산소포화도로 정의되는 저산소증, 무호흡 시간, 그리고 20% 이상의 심박수, 혈압, 기도압력 상승이 증가했다). 또한 입력 변수 중 기도 압력이 인공호흡 제어에 가장 중요한 요소로 확인되었다.
결론적으로, AIVE 모델은 마취 응급상황에서 임상의의 인공호흡 조절 정책보다 합병증을 줄이면서 더 높은 보상을 달성할 수 있었다.
이번 연구는 인공지능 알고리즘의 일종인 강화학습을 의학 분야에 적용한 연구로, 새로운 모델을 개발하기 위해 실제 임상 현장에서 수집된 대규모 생체 신호 데이터를 활용하였으며, 다기관 데이터로 검증을 하였다. 이를 통해 임상적 이용 가능성을 제시하는 우수한 연구 결과를 얻을 수 있었다.
Impact of treatment on long-term survival of patients with mycobacterium avium complex pulmonary disease
Clinical Infectious Diseases, 2023

(내과학교실,교신저자)

(서울대학교병원 내과,
제1저자)
내과학교실 임재준 교수와 서울대병원 호흡기내과 김중엽 교수팀은 Mycobacterium avium-complex 폐질환에 대한 항생제 치료가 환자들의 장기적인 생존에 미치는 영향을 분석하고 결과를 미국 감염학회 공식 저널에 출판하였다.
M. avium-complex는 결핵균을 제외한 마이코박테리아 중에서 만성 폐질환을 일으키는 가장 흔한 균으로, 최근 들어 그 유병률과 발병률이 크게 증가하여 중대한 의학적 문제로 대두되고 있다. 치료는 마크로라이드계 항생제에 2-3가지 다른 계열의 항생제를 병용하는 것으로, 국제지침에서는 호흡기 검체에서 더 이상 균이 배양되지 않게 된 후에도 12개월 이상 치료를 유지할 것을 권고하고 있다. 그러나 완치율은 60%에 불과하고, 17-75%의 환자들이 항생제로 인한 부작용을 경험하며, 아직 이러한 장기 치료가 생존율을 개선시킨다는 연구는 없는 상태이다.
이에 연구팀은 2009년 1월부터 2020년 12월 사이 서울대학교병원에서 M. avium-complex 폐질환으로 치료를 시작한 486명의 환자의 항생제 노출 기간에 따른 생존율을 시간 종속 다변량 콕스 비례 위험 모델(Time-varying multivariable Cox proportional hazards model)을 이용해 계산하였다. 성별, 연령, 체질량지수, 동반 질환과 질병 관련 인자[공동(cavity) 형성 여부, 항산균 도말 검사 결과, 약제 감수성 결과, 적혈구침강속도 등]를 보정한 상태에서 분석한 결과, 환자들의 생존율은 치료 기간이 길어질수록 증가하였고, 18개월 이상 치료받은 환자는 3개월 미만으로 치료받은 환자에 비해 사망률이 68% 감소하였다. 특히, 이러한 장기 치료에 의한 생존율 개선 효과는 치료 시작 시점에 항산균 도말 검사 결과가 양성이거나, 영상학적으로 공동(cavity)이 형성된, 즉, 질병의 중증도가 더 높은 하위 집단에서 두드러졌다.
지금까지 M. avium-complex 폐질환에서 항생제 치료는 완치율이 높지 못하고 생존율을 개선시킨다는 근거가 부족하여 환자들에게 적극적으로 권해야 하는지, 아니면 빈번한 부작용 발생 등을 고려하여 최대한 보류하고 능동적 감시(watchful waiting)를 해야 하는지 학계 내 의견이 분분하였다. 이에 이번 연구 결과는 해당 질환에서 장기 항생제 치료가 환자들의 생존에 긍정적 영향을 미친다는 것을 보여주어 임상적 의의가 크다.

