[연구동향]
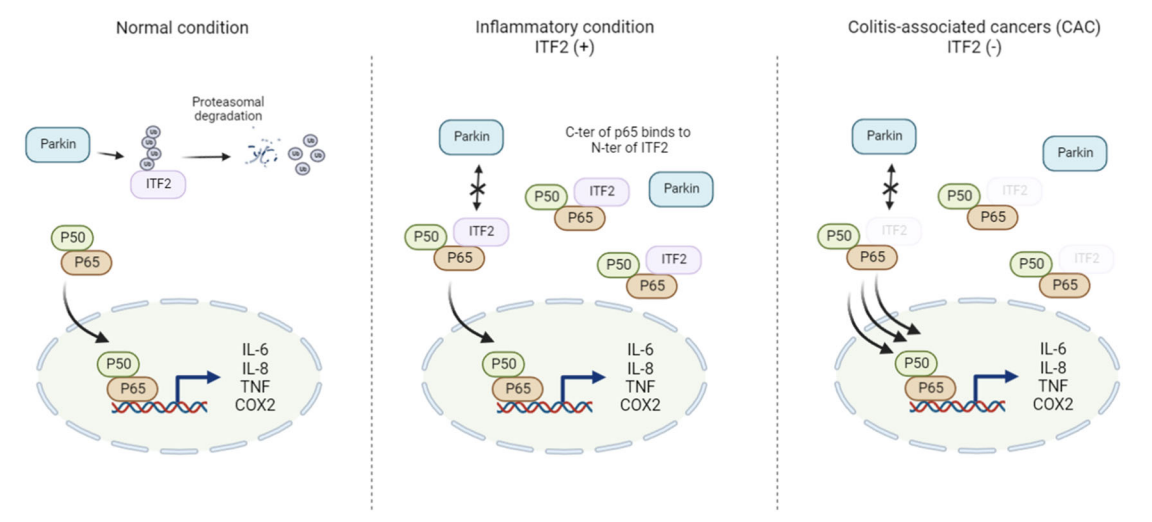
Protein stabilization of ITF2 by NF-κB prevents colitis-associated cancer development
nature communications, 2023

(약리학교실,교신저자)

(하버드대학교,공동제1저자)

(의과학과,공동제1저자)
지속적인 염증은 암의 특징이며 종양 형성과 강하게 연관되어 있지만 근본적인 분자 메커니즘은 잘 알려져 있지 않다. 염증 상태는 Ex vivo와 in vitro 모두에서 ITF2 및 p65 발현을 증가시켰고, ITF2와 p65의 발현은 양의 상관관계를 보였다. p65 과발현은 E3 ligase인 Parkin과 ITF2의 결합을 방해함으로써 ITF2 단백질 수준을 안정화시켰다. 구체적으로, p65의 C말단은 ITF2의 N말단에 결합하여 유비퀴틴화를 억제함으로써 ITF2 안정화를 촉진하였다. ITF2가 장 상피세포 특이적으로 결실된 쥐에서는 p65의 핵 전좌를 촉진하여 Azoxymethane (AOM)/Dextran sulfate sodium (DSS) 또는 DSS에 의해 매개되는 대장염 관련 암 종양 형성이 증가되어 있었다. ITF2 발현은 대장염 관련 암 환자의 종양 조직에서 소실된 반면, p65 발현은 이형성 및 종양 조직 모두에서 훨씬 더 증가되어 있었다. 본 결과는 2014년 Gastroenterology에 게제된 ITF2의 대장암 발병 기전의 후속 연구로서, 돌연변이와 염증이라는 두가지 요소가 모두 작용하는 대장암의 발병 과정에서 과도한 염증에 의한 종양 발생을 억제하는 내인적 억제 기전을 제하였다는 의미가 있다. 따라서 이러한 발견은 대장염 관련 암 진행의 억제에서 ITF2의 중요한 역할을 나타내며 ITF2는 대장염 관련 암을 포함한 염증성 질환에 대한 중요한 치료 타겟이 될 수 있음을 보여준다. 본 연구는 한국연구재단의 기초연구실 지원사업 및 중견연구 지원사업을 통해 수행되었다.
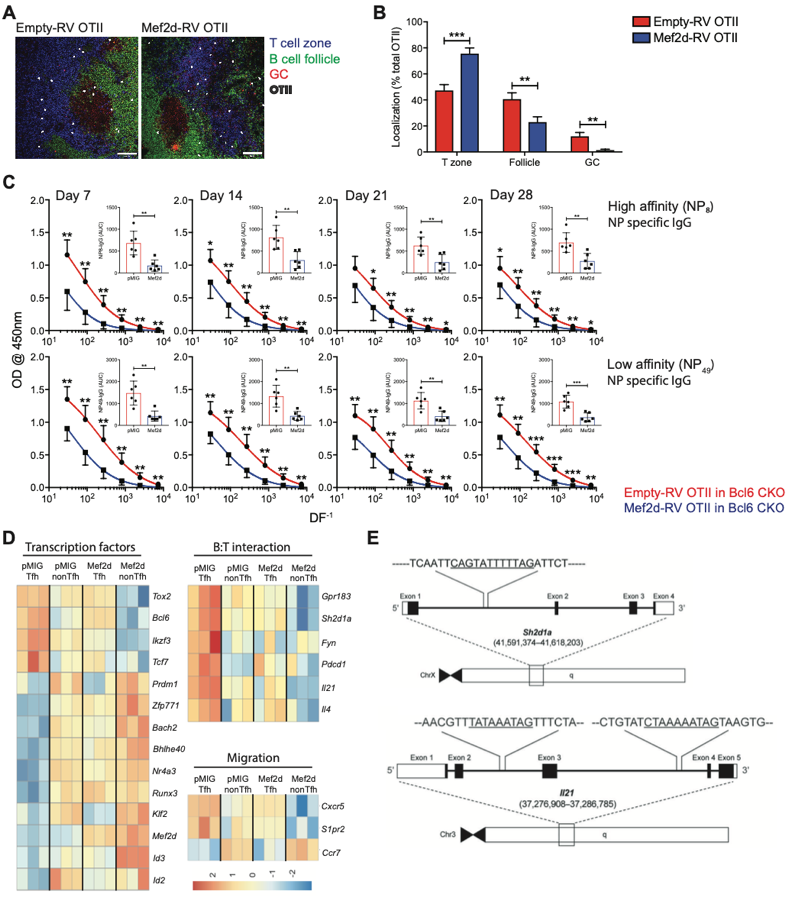
The transcription factor Mef2d regulates B:T synapse-dependent GC-Tfh differentiation and IL-21-mediated humoral immunity
Science Immunology, 2023

(의과학과·의학과,교신저자)

(의과학과,제1저자)
백신을 통한 강한 결합력을 가진 항체의 생성은 병원체를 효과적으로 제거할 수 있도록 도움을 주지만, 자가 항원에 대한 강한 결합력을 가진 항체의 생성은 자가면역 질환을 유발하는 원인이 될 수 있으므로 항체 생성 반응은 면역체계에 의하여 정밀하게 조절되어야 한다.
종자중심반응은 강한 결합력의 항체를 생성하는 B 세포의 발달에 매우 중요한 면역학적 과정으로, B 세포와 여포보조 T (Tfh) 세포의 항원 특이적 상호작용을 통해 종자중심이 발달 및 유지되고 이 과정에서 항원에 높은 결합력을 갖춘 B 세포가 선택된다. 이러한 “B 세포 – Tfh 세포” 상호작용은 신경세포에서 발견되는 것과 유사한 구조, 즉 시냅스를 통해 일어나고, 면역시냅스는 T 세포 수용체:주조직 적합성 복합체, 보조자극분자, 접착분자들의 결합으로 이루어진다. Tfh 세포 내에서 기능하는 SAP 단백질은 접착분자인 SLAM 단백질 하위에서 신호를 전달하는 어댑터 단백질로 B 세포와의 시냅스 유지에 절대적으로 필요하고, 따라서 B 세포의 종자중심반응의 형성에 중요한 역할을 하지만, SAP 단백질의 발현 조절 메커니즘은 아직 명확히 밝혀지지 않고 있다.
본 연구에서는 신경세포의 시냅스 형성을 저해하는 Mef2d 전사인자가 면역계의 “B 세포 – Tfh 세포” 시냅스 형성을 억제함으로써 Tfh 세포 분화와 B:T 시냅스 의존적인 종자중심 발달을 저해하고, 그 결과 체액성 면역 반응을 제한하는 면역기능을 수행하는 것을 규명하였다. 논문의 1저자인 김예지 학생(대학원 의과학과)은 Mef2d의 Gain-of-function, Loss-of-function 연구와 분자생물학, 생화학, 그리고 RNA-seq 분석 기반 기전연구를 수행하였고, 이를 통해 CD4 T 세포에서 Mef2d 전사인자가 SAP 단백질을 코딩하는 Sh2d1a 유전자의 발현을 직접적으로 저해하는 것을 확인하였다. 이로 인하여 항원 특이적 B 세포의 종자중심반응이 저해되고, 궁극적으로 항원과 높은 결합력을 갖는 항체의 유도가 억제되는 것을 확인하였다. 또한, Mef2d 전사인자는 종자중심반응을 포함, CD4 T 의존적 체액성 면역의 유도에 중요한 역할을 하는 도움 분자로 알려진 IL-21 사이토카인의 분비를 직접적으로 억제하는 것을 확인하였다. 비정상적 종자중심반응 유도와 IL-21 사이토카인 형성이 루푸스와 같은 자가면역질환에서 확인되는데, 루푸스 환자와 대조군의 CD4 T 세포를 분석함으로써 CD4 T 세포에서 Mef2d의 발현이 루푸스 환자에서 대조군에 비해 낮아져 있고, 이는 루푸스 환자의 자가 항체 형성을 포함한 자가면역질환 척도들과 “negative correlation”이 있는 것을 확인하였다.
이 연구를 통해 다세포로 구성된 신경계와 면역계가 개체의 내/외부에서 일어나는 변화에 적절히 대응하는 것을 지원하기 위해 갖춘 “시냅스”를 조절하기 위하여 전사적 조절 기전을 공유하고 있는 것이 처음 밝혀졌고, Mef2d 전사인자의 발현 및 기능 조절 기전을 규명함으로써 항원 특이적 B 세포의 체액성 면역 반응을 제어할 수 있는 가능성을 제시한다.
논문링크 : https://www.science.org/doi/10.1126/sciimmunol.adf2248
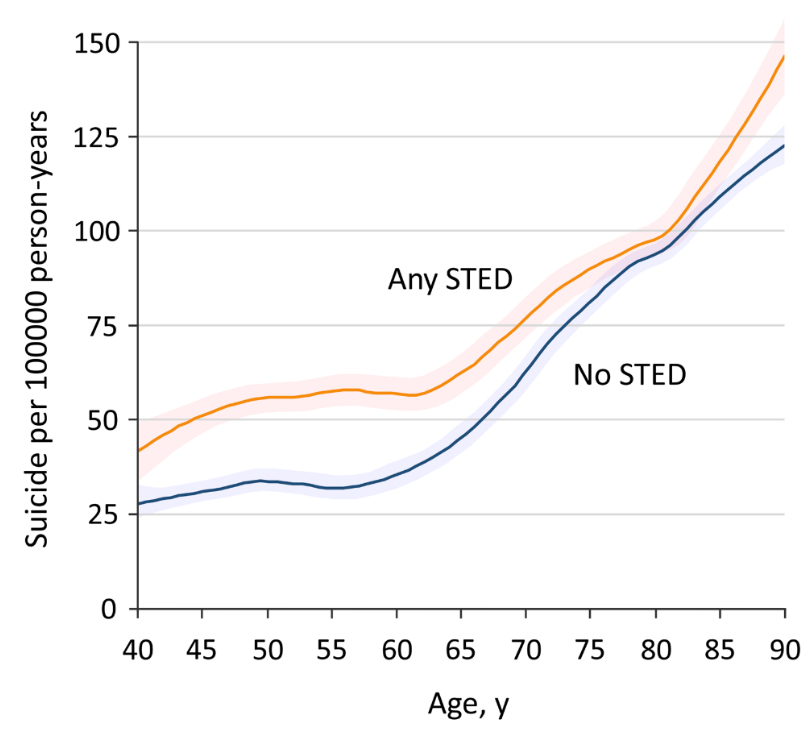
Association between Sight-Threatening Eye Diseases and Death by Suicide in South Korea: A Nationwide Population-based Cohort Study
Ophthalmology, 2023

(안과학교실,공동교신저자)

(의공학교실,공동교신저자)

(서울대학교병원 의생명연구원,
공동제1저자)
이번 연구는 건강보험 청구 데이터를 활용해 2010-2020년 실명유발 3대 안과질환으로 진단받은 군에서 자살 발생 위험을 분석한 연구이다.
초기 증상을 자각하기 어렵고 치료 시기를 놓치면 실명의 위험이 있는 3대 안과질환은 당뇨, 고혈압 등의 기저질환을 앓는 인구가 늘어나고 인구 고령화가 진행됨에 따라 지속적으로 증가하고 있다. 시력 장애와 자살 위험과의 연관성을 분석한 기존 연구가 존재하나 주요 안질환 환자에서의 자살 위험을 규명한 연구는 없었다. 이번 연구에서는 환자의 성별, 연령, 소득수준, 거주지역, Charlson Comorbidity Index 등 자살에 연관된 요인들을 통제하고 3대 안과질환 진단, 시력장애, 나이에 따른 자살 위험을 산출해 비교 분석하였다.
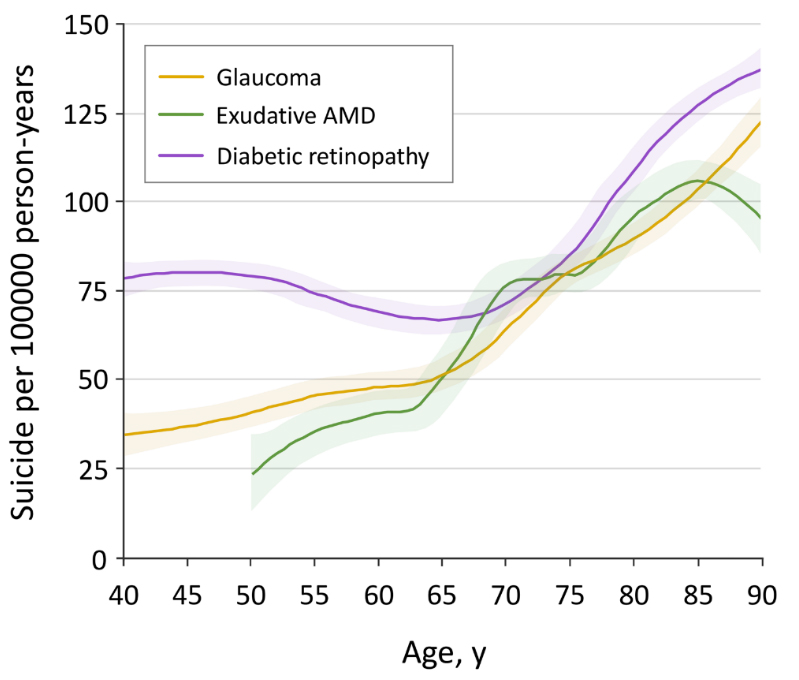
3대 안과질환 환자의 연령별 자살 사망률은 나이가 들수록 증가하였으며 진단 시점부터 자살 위험도를 비교한 결과 비환자군보다 꾸준히 높은 것으로 나타났다. 녹내장, 나이관련 황반변성, 당뇨망막병증 환자의 자살위험도는 각각 1.09배, 1.2배, 1.4배 증가했으며 하나 이상의 안과질환을 앓고 있는 환자의 경우 자살 위험도가 1.33배 증가했다. 또한 하나 이상의 3대 안과질환을 진단받은 환자가 시력장애 판정을 받은 환자의 경우 자살 위험도가 1.49배로 증가하였으며 65세 이하의 당뇨망막병증을 진단받은 환자의 경우 자살 위험도가 2.04배 증가한 것으로 분석되었다.
최초 3대 안과질환 진단 시점에 따른 자살 위험도 분석 결과 최초 진단시점부터 6개월까지 자살위험도가 증가하여 3개월~6개월 사이의 자살 위험도가 5.33배로 매우 높았으며 이후 감소하는 것으로 나타났다.
점점 더 심각해지는 한국의 높은 자살율은 사회 전반적인 문제이며 3대 안과질환은 환자에게 상당한 심리적 영향을 미치기 때문에 질환과 자살의 인과관계 및 경로를 정확하게 규명하는 것은 향후 안과질환으로 인한 자살 위험군에 대한 주치의의 주의 깊은 관심과 관리의 필요성을 일깨우고 자살 예방대책 수립 및 지원체계를 구축하는데 있어서 큰 도움이 될 수 있다.
Earlier age at type 2 diabetes diagnosis is associated with increased genetic risk of cardiovascular disease
Diabetes Care, 2023

(의학과,공동교신저자)

(분자의학 및 바이오제약학과,
공동교신저자)

(중개의학교실,제1저자)
국내 30세 이상 성인 당뇨병 환자수는 526만 명으로 추산되며, 이는 6명 중 1명 꼴이다. 특히 이들 중 30대, 40대에 당뇨병을 진단받는 사람이 93만 명으로 전체 성인 당뇨병 환자 중 18%를 차지하며, 전세계적으로 젊은 나이에 당뇨병이 발병하는 사람들이 늘고 있다.
조기에 당뇨병이 진단된 사람들은 늦은 나이에 진단된 사람들보다 당뇨병 진행 속도가 빠르고 합병증 발생 위험이 더 높다. 그러나 왜 젊은 당뇨병 환자들에게서 이러한 합병증 발생 위험이 더 높은지는 잘 알려지지 않았다. 본 연구진은 당뇨병 발병 연령에 유전적 요인이 강하게 작용한다는 점에 착안하여, 유전적 요인이 조기 발병 당뇨병 환자의 심혈관질환 위험을 높일 것이라는 가설을 세우고 연구를 실시하였다.
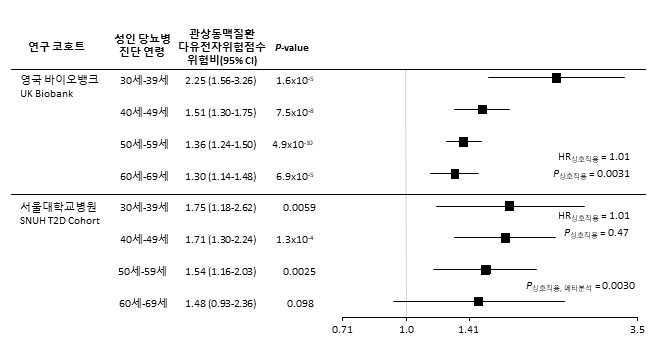
먼저 연구팀은 영국 바이오뱅크 코호트에 등록된 당뇨병 환자 1만 2321명의 유전자를 분석해 대표적인 심혈관 합병증인 관상동맥질환과 관련된 유전자변이들을 확인하고, ‘다유전자위험점수’로 정량화했다. 이 점수가 높을수록 관상동맥질환이 발생할 유전적 위험이 크다고 알려졌다. 이후 당뇨병 환자를 진단 연령별로 13년간 추적 관찰하고, 다유전자위험점수를 이용하여 ‘관상동맥질환 발생에 대한 유전적 영향의 크기’를 의미하는 위험비(HR)를 확인했다.
그 결과, 진단 연령이 10년씩 빨라질 때마다 관상동맥질환의 위험비가 14%씩 증가하는 경향이 확인됐다. 30대 당뇨병 진단 그룹의 위험비(HR 2.25)는 60대(HR 1.30)에 비해 1.73배 높았다. 이 결과는 서울대병원 코호트에 등록된 1165명의 당뇨병 환자를 8년간 추적 관찰했을 때도 유사했다.
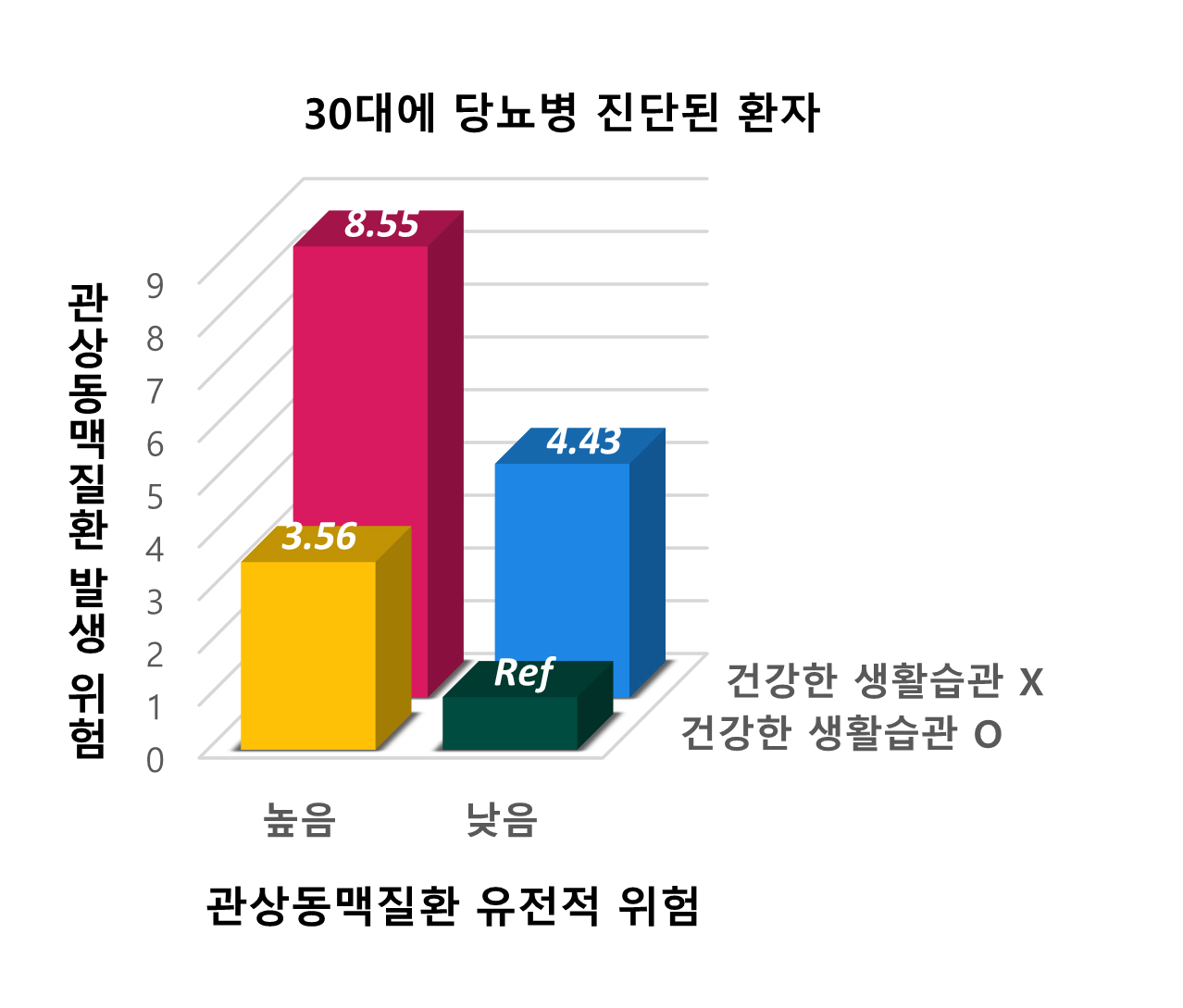
또한, 젊은 당뇨병 환자들의 심혈관질환 위험도를 낮추는데 있어서 건강한 생활습관을 갖는 것이 낮은 유전적 위험도를 갖는 것과 비슷한 효과가 있었다. 즉, 유전적으로 심혈관질환의 위험이 높아도 건강한 생활습관을 통해 그 위험을 감소시킬 수 있었다.
이번 연구를 통해 젊은 나이에 당뇨병이 발병하는 환자들은 심혈관질환의 위험이 증가하는데, 그 원인 중 하나로 유전적인 요인이 있다는 사실을 확인했다. 특히 건강한 생활습관은 이러한 유전적 위험을 감소시킬 수 있었다. 향후 젊은 당뇨병 환자들의 유전자 분석을 통해 심혈관질환이 높은 사람을 미리 선별하고, 생활습관개선을 통해 심혈관질환 발생을 낮추는 ‘정밀 의료’가 실현 가능할 것으로 기대된다.
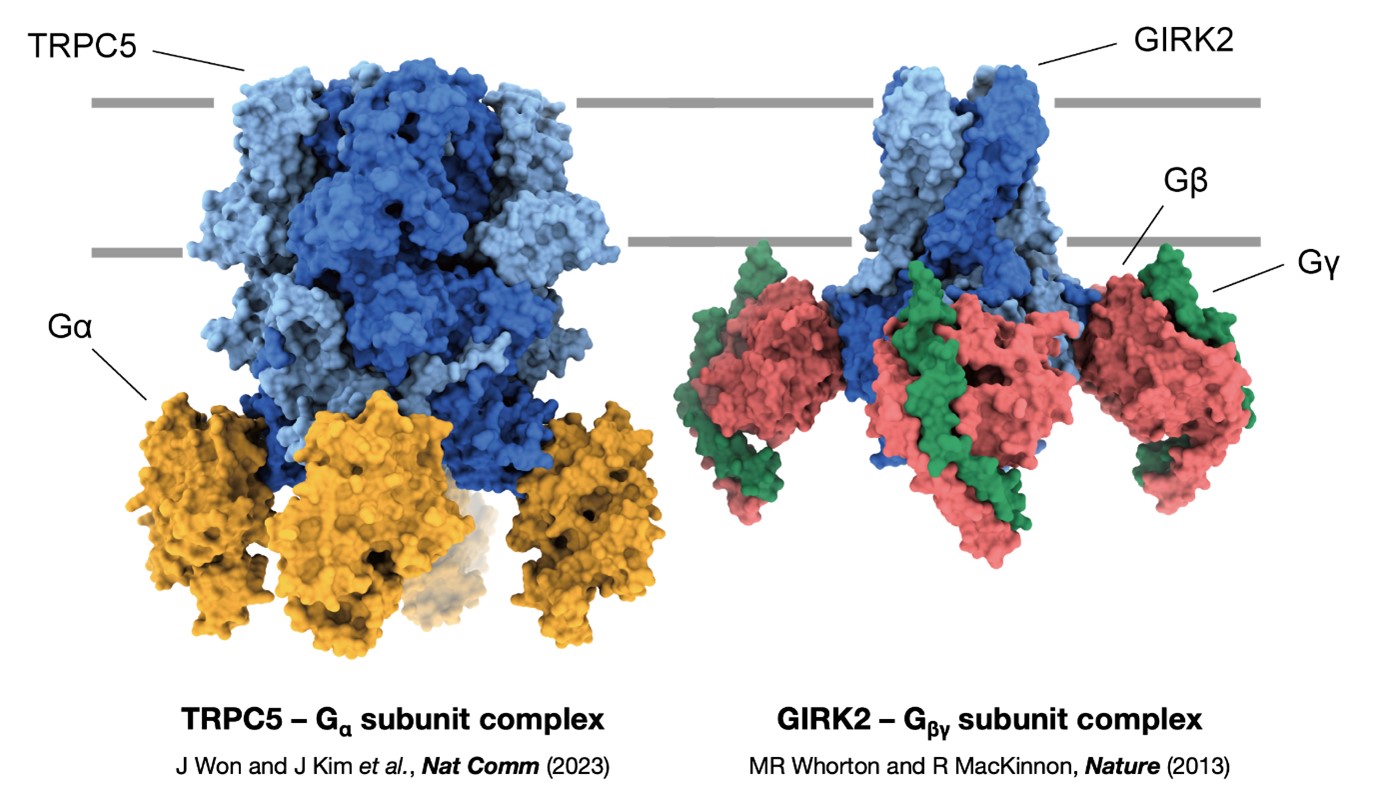
Molecular architecture of the Gαi-bound TRPC5 ion channel
nature communications, 2023

(생리학교실,교신저자)

(생리학교실,제1저자)
G-protein coupled receptor (GPCR)과 이온통로는 대표적인 막관통단백질들로, 이들의 정상적인 작동은 세포 외부의 자극이 세포
내부로 변환되고 전달되기 위해 필수적이다. 그동안 G-단백질의
α 단위체(Gα subunit)가 이온채널을 직접적으로 활성시킬 수 있다는 가능성이 지속적으로 제시되었으나 이것에 대한 구조적 증거는 전무하였다.
본 논문에서는 서울대학교 의과대학 생리학교실 서인석 교수 연구팀과 서울대학교 자연과학대학 화학부 이형호 교수 연구팀의 공동연구를 통해
동결현미경(cryogenic electron microscopy, cryo-EM) 기법으로 규명한 TRPC5-Gαi3 복합체의 3차원적 구조를 소개하고, 이를 기반으로 실시된 이온채널의 기능적 조절기작에 관한 실험과 분석을 밝혔다.
복합체의 3차원적 구조를 바탕으로 연구진은 4개의
Gαi3가
TRPC5 채널의 ankyrin repeat domain (ARD)에 결합하는 것을 확인하였다. Gαi3가 TRPC5에
결합한 복합체로서의 채널 구조를 확보하였지만, selectivity filter 및 lower gate를 포함하여 채널 중심의 구조를 자세히 분석하였을 때 여전히 채널은 닫힌 상태인 것으로 확인되었다. 이 발견은 전기생리학적 결과와 일치하였는데 즉, 세포 안쪽에 PIP2가 공급되지 않으면 Gαi3 독자적으로는 채널이 열릴 확률(open probability, Po)을 크게 증가시키지 못한 결과와 같은 맥락을 이루었다. 결국 Gαi3의 결합이 실질적인 채널의 열림을 유도하기 위해서는 반드시 채널에 PIP2가
결합되어야 한다고 생각하였고, 따라서 Gαi3의 결합, PIP2의 결합, 그리고
Po사이의 열역학적 상관관계를 분석하였다. 결론적으로
Gαi3 결합의 효과는 TRPC5 채널의 PIP2에 대한 해리상수(dissociation
constant, KdPIP2)를 낮추는 것으로 나타났다.
Gαi3가 없을 때에 KdPIP2는 23.3 ± 1.0 mM이었던 것에 반해, Gαi3가 있을 때에는 10.2 ± 1.0 mM로 나타났다. 후자는 세포 내 생리학적인 PIP2
농도(4-10 mM)와 유사하며, 이 농도에서 Gαi3의 Po 증가효과가 가장 크게 발휘되는 것으로 나타났다.
종합적으로, 본 논문에서 제시된 결과를 토대로 공동 연구진은 다음과 같은 결론을 도출하였다. 첫째, 세포막에 국한된 여타 효소들에 더하여 이온채널은 Gα 단백질에 의해 직접적으로 기능이 조절되는 직접효과인자(direct
effector molecule) 중 하나로 여겨질 수 있다. 둘째, GPCR과 이온채널 사이의 기능적 상호작용을 매개하는 인자로서(Gbg 단위체의 결합 혹은 G-단백질 하위 이차전령체계에 의한 간접적 조절에 더하여) Gα 단위체에 의한 직접적 상호작용을 충분히 고려하여야 한다. 이러한
시각은 지금까지 알려지지 않았거나 해석되지 않았던 두 막관통단백질 군 사이의 기능적 상호작용을 풀어낼 수 있는 새로운 접근법이 될 것으로 기대한다.