[연구동향]
A logical network-based drug-screening platform for Alzheimer’s disease representing pathological features of human brain organoids
Nat Commun, 2021

박종찬 박사후연구원 (제1저자)

이동준 박사과정생 (제1저자)

묵인희 교수(생화학교실, 교신저자)
알츠하이머병은 뇌 속에 비정상적으로 축적되는 세포독성 베타-아밀로이드와 타우 단백질에 의해발생하는 질환이라고 알려져 있다. 하지만 실제 살아있는 환자의 뇌는 검체획득이 어렵기 때문에, 약물 실험에 있어서는 실제 환자유래의 유도만능줄기세포를 이용한 뇌 오가노이드의 분화가 필수적이라고 볼 수 있다. 본 연구진은 근본적인 질병 치료를 위한 약물의 타겟 후보를 결정하기 위해, 질병의 생물학적 메커니즘에 대한 동역학 분석을 기반으로 한 시스템생물학 연구와의 융합을 시도하였다. 이러한 과정을 통해 최종 선별된 6종의 약물 조합으로 실제 환자 유래 뇌 오가노이드 1300여개를 이용하여 고효율 High-Content Screening (HCS) 이미징 기법을 통해 대량의 뇌 오가노이드 샘플을 빠른 시간 내에 약효평가를 할 수 있는 시스템을 구축하였다. 선별된 약물들을 HCS장비로 약효를 평가한 결과, 알츠하이머병 뇌 오가노이드 및 CRISPR-Cas9 변형 오가노이드에서 뇌 속 베타 아밀로이드와 타우의 축적이 감소됨을 확인하였다. 이는 선정된 약물 타겟 후보들에 대하여 실제 환자의 뇌 속 베타 아밀로이드와 타우 축적을 약화시키는 효능이 있음을 실험적으로 검증하였음을 의미한다. 이번 연구는 세계 최초로 시스템생물학 기반 컴퓨터 모델을 개발하고 이를 환자 유래 뇌 오가노이드를 통하여 검증한 사례로써, 알츠하이머병에서도 환자가 지닌 유전적 위험요인을 고려한 환자별 최적의 약물 효능 예측 및 타겟 발굴에 기여할 것으로 기대된다.
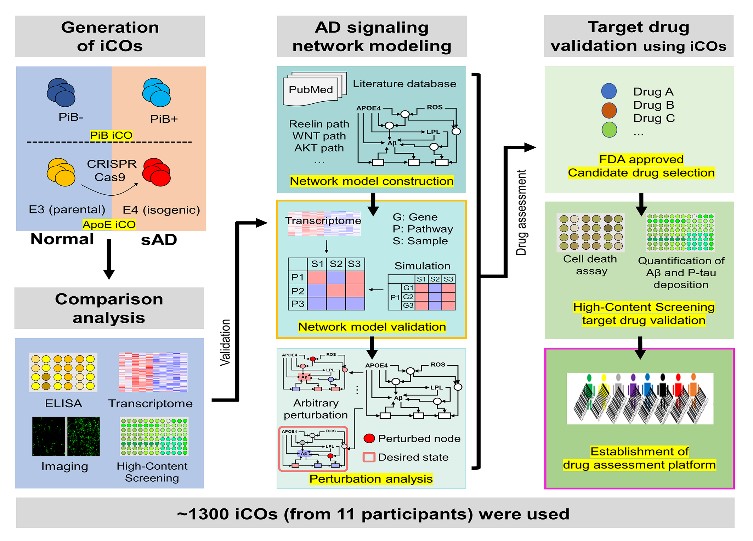
본 연구의 전체 흐름을 보여주는 모식도
Topological Data Analysis of Coronary Plaques Demonstrates the Natural History of Coronary Atherosclerosis
JACC Cardiovasc Imaging, 2021

이승표 교수(내과학교실)

황도연 전임의(서울대학교병원 내과)
관상동맥질환은 심장에 혈액을 공급하는 관상동맥의 동맥경화로 인해 발생하는 여러 질환을 포괄하는데 안정형 협심증, 불안정형 협심증 그리고 급성심근경색 등으로 발현합니다. 전세계적 사망 원인 중 가장 많은 비율을 차지하는 질환 중 하나이며 이를 어떻게 진단하고 이것이 어떠한 임상 사건과 연계되어 있는지를 예측하는 것이 매우 중요하겠습니다. 기술의 발전과 함께 컴퓨터 단층촬영 (CT, computed tomography)이 의료에서 활발히 사용되고 있으며 이를 이용한 관상동맥질환자의 진단 그리고 예후 예측이 활발히 연구되고 있습니다.
관상동맥 컴퓨터 단층촬영 (CTA, coronary computed tomography)을 통해 기존의 연구들에서는 동맥경화반의 정도 (atherosclerosis plaque burden), 혈관의 양성 재형성 (positive remodeling), 혈관의 점성 석회화 (spotty calcification), 그리고 저음영 동맥경화반 (low attenuation plaque) 등과 같은 소견들이 환자의 예후와 관련 있었습니다. 하지만, 관상동맥질환이 진행하는 복잡한 과정을 생각해 볼 때 이런 단편적인 특성이 질환의 병태 생리를 모두 설명하기에는 역부족입니다. CTA에서 우리는 이런 단편적 정보를 포함하여 다양한 정보를 얻을 수 있는데, 이를 통해 복잡한 관상동맥질환의 진행 과정 및 예후를 잘 설명할 수 있을 것으로 생각이 되고, 데이터 과학의 발달로 다양하고 복잡한 데이터를 보다 통합적으로 해석 가능합니다.
본 연구에서는 위상학적 자료 분석 (TDA, topological data analysis)을 활용하여 CTA를 통해 확인되는 전체 관상동맥의 동맥경화반 부피 (plaque volume) 그리고 동맥경화반의 구성 (plaque composition)이 질병을 이해하고 환자의 예후를 예측하는 데 도움이 될 것이라는 가설 하에 진행되었습니다 (그림). TDA를 통해 네트워크에 기반한, 환자-환자 유사성 모델 (network-based patient similarity model)을 만들어, 본 연구에서는 현재 임상에서 단편적으로 이해하고 있는 관상동맥질환이 연속적인 과정을 통해 다양하게 진행하는 질환이며 환자들도 크게 3 개의 그룹으로 나누어 생각해 볼 수 있다는 것을 확인할 수 있었습니다. Group A는 상대적으로 초기의 동맥경화를 보이는 환자들로 전체적인 Plaque volume도 적고 Lipid component와 Calcium component가 적은 환자들이었고, Group B는 조금 더 진행된 형태의 환자들로 중등도의 Plaque volume을 가지면서, Lipid component가 많은 환자들이었습니다. 마지막으로 Group C는 진행된 형태의 동맥경화를 보이는 그룹으로 가장 많은 Plaque volume을 가지면서 Calcium component가 가장 많이 확인되는 환자들이었습니다.
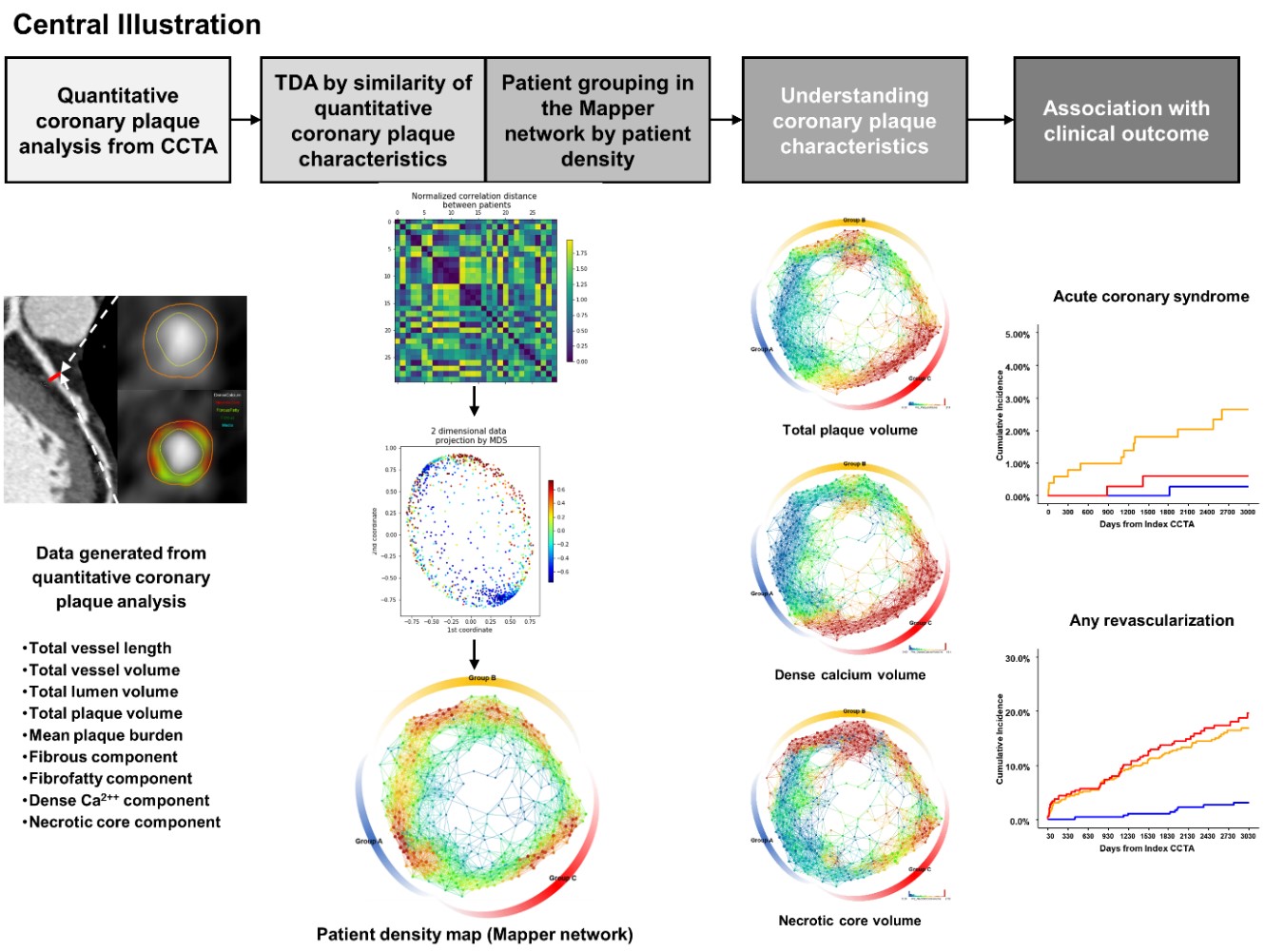
그림. 관상동맥 컴퓨터 단층촬영 (CTA, coronary computed tomography)에서 확인되는 관상동맥 및 동맥경화에 대한 정보를 위상학적 자료 분석 (TDA, topological data analysis)을 통해 Network based patient similarity model을 만들었다. 이를 통해 세 개의 서로 다른 환자군이 있음을 확인하였으며 예후 또한 차이가 났음을 확인하였다.
TDA 통해 확인한 세 개의 그룹은 공통된 특징을 공유하고 더 나아가 환자 예후 및 임상사건에서도 서로 다른 양상을 보여줌으로써 임상적 가치를 입증할 수 있었으며, TDA로 확인한 관상동맥질환의 설명 모델에서 질환의 진행이 Group A에서 Group B를 거쳐 Group C로 진행할 수도, Group A에서 Group C로 바로 진행할 수도 있다는 가설을 확인해 볼 수 있었습니다.
이번 연구를 통해 새로운 데이터 분석 기법을 통해 관상동맥질환을 새로이 이해하는 모델을 수립할 수 있었으며 관상동맥질환의 상태를 판단하고 예후를 예측하는 데 있어 새로운 방식을 제시했다는 점에서 의미가 있다고 볼 수 있습니다. 해당 연구는 이에 미국심장학회지 공식 이미징 저널인 'Journal of the American College Of Cardiology Cardiovascular Imaging (IF 12.74)' 1월호에 게재되었습니다.
논문링크
https://www.sciencedirect.com/science/article/pii/S1936878X20310147
Genome-wide association study of non-tuberculous mycobacterial pulmonary disease
Thorax, 2021

조재영 교수(서울대학교병원 호흡기내과)

임재준 교수 (내과학교실)
비결핵항산균(Non-tuberculous mycobacterium, NTM) 폐질환은 전세계적으로 발병률이 계속 증가하고 있다. 결핵균과 달리 비결핵항산균은 토양과 강물 등의 자연환경에 널리 분포하고 있으므로 거의 모든 사람들이 종종 비결핵항산균을 흡입하게 되는데, 이들 중 일부에서만 비결핵항산균 폐질환이 발생한다. 이 점은 비결핵항산균 폐질환에 대한 유전적 소인이 존재한다는 점을 시사하지만, 그 동안 밝혀내기 쉽지 않았다.
연구진은 보건대학원 원성호 교수팀과 함께 비결핵항산균 폐질환의 유전적 소인을 규명하기 위해 전장유전체 연관분석 연구 (genome-wide association study)를 시행했다. 400여 명의 서울대병원 비결핵항산균 폐질환자와 비슷한 수의 건강 대조군으로 구성된 코호트를 분석해서 7번 염색체에 위치한 rs849177라는 단일염기변형(single nucleotide polymorphism)이 비결핵항산균 폐질환의 발생과 관련이 있다는 것을 찾아냈다. 또한 연관된 유전자 발현을 찾기 위한 다수의 분석에서 rs849177이 STK17A라는 유전자의 발현과 관련이 있다는 것을 밝혔다. STK17A는 세포자멸사(apoptosis)를 촉진하는데, rs849177라는 단일염기변형을 가지고 있는 환자는 STK17A의 발현이 감소되어 있다. 이에 비결핵항산균에 감염된 대식세포가 자멸하지 못하고, 비결핵항산균은 대식세포 안에서 살아남아, 환자는 이 질병에 취약해질 것으로 생각된다.
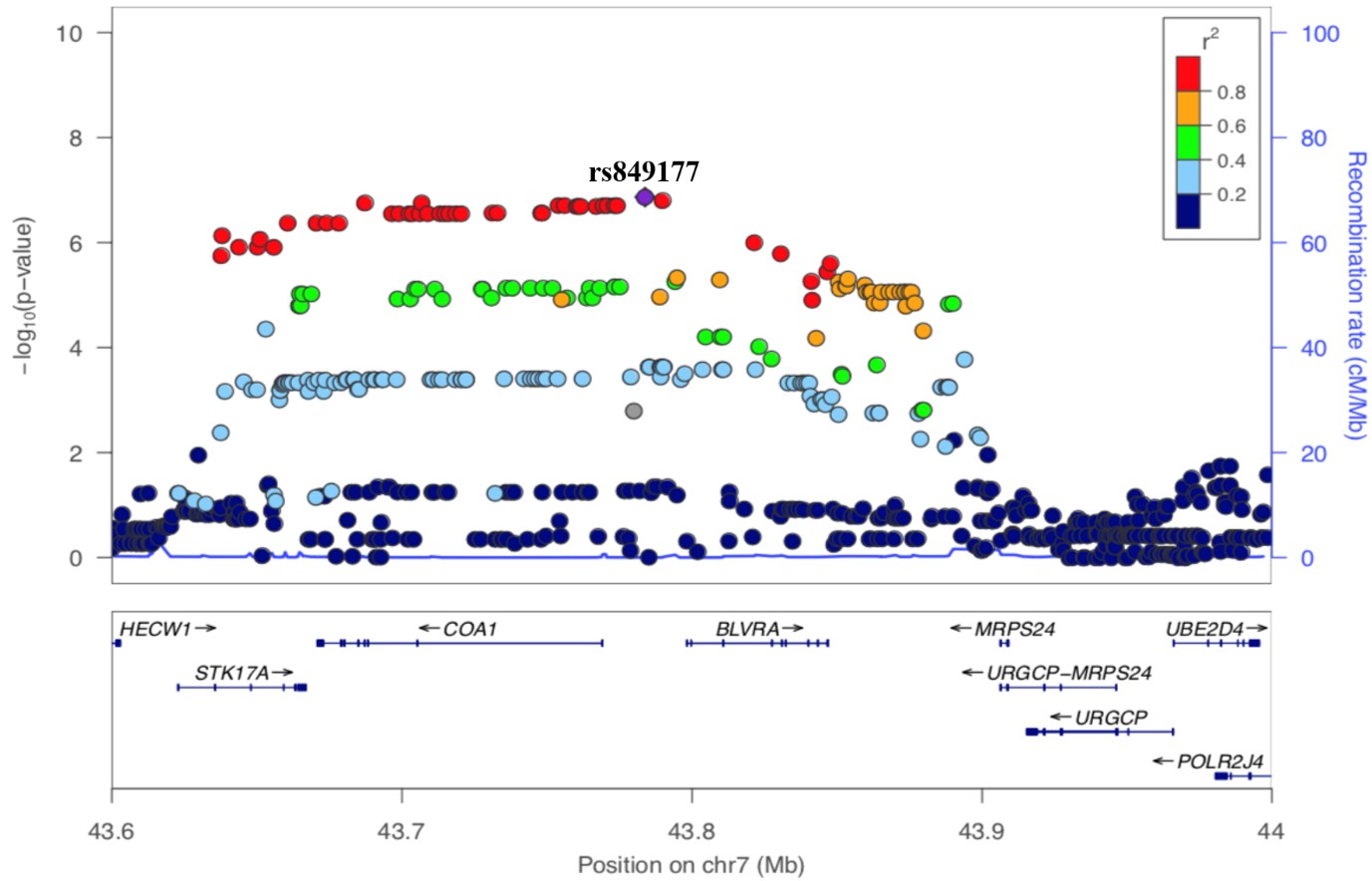
그림. rs849177과 STK17A를 포함한 주변 유전자를 한 눈에 보여주는 regional plot
SCAMP5 plays a critical role in axonal trafficking and synaptic localization of NHE6 to adjust quantal size at glutamatergic synapses
Proceedings of the National Academy of Sciences of the United States of America (PNAS), 2021

이웅휘 대학원생 (제1저자)

장성호 교수 (생리학교실)
연평균 8%씩 환자수가 증가하고 있는 자폐증 등 뇌발달장애는 완벽한 기전 및 치료법이 알려지지 않아 연구가 지속적으로 진행되고 있다. 최근까지 자폐성 뇌발달장애는 대부분 다양한 유전자들의 돌연변이에 의한 신경세포의 시냅스 구조변이가 발병 원인으로 보고돼 왔지만, 신경전달물질 분비에 관여하는 단백질의 돌연변이가 어떤 기전을 통해 신경전달물질 분비를 저해하여 자폐증에서 발견되는 신경기능저하를 유도하는가는 전혀 알려져 있지 않았다.
서울대학교 의과대학 장성호 교수 연구팀(제1저자 : 이웅휘 대학원생)은 뇌신경세포에서 자폐증 원인 단백질로 알려진 SCAMP5와 NHE6의 상호작용 억제 시, 흥분성 신경세포의 신경전달물질인 글루타메이트의 시냅스 소포 충전에 중요한 NHE6의 단백질 발현 위치에 이상이 생기고 결국 시냅스 전 뉴런에서 글루타메이트의 분비량이 현저히 감소해 시냅스의 신경신호전달 및 생리학적 기능에 심각한 문제를 초래한다는 기전을 규명했다.
기존에는 서로 관련이 없는 것으로 알려졌던 두 자폐증 원인 단백질들이 대뇌 신경세포에서 직접적 상호작용을 통해 신경전달물질 분비조절에 관여한다는 것이 밝혀짐으로써 차후 자폐성 발달장애에 관여하는 다양한 단백질들의 기능을 개별적이 아닌 통합적인 측면으로서 연계연구를 통해 공통 기전을 규명해야 한다는 점을 제시하는 중요한 연구이다.
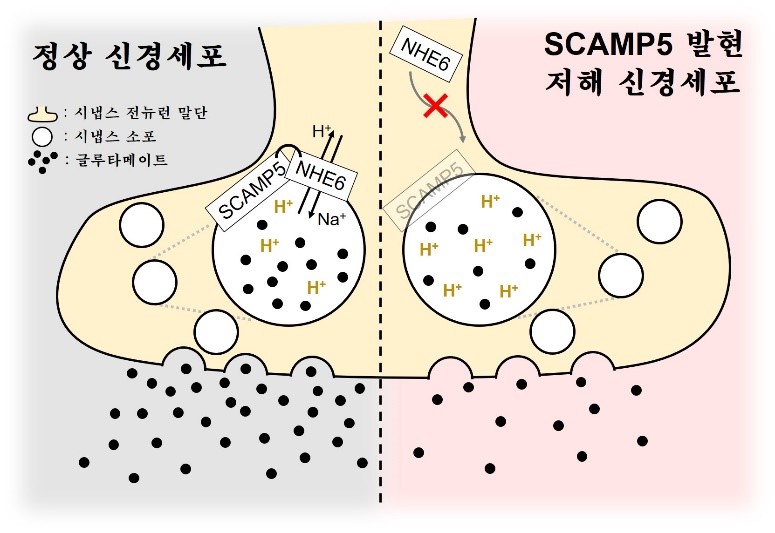
그림 1. 뇌신경세포에서 SCAMP5와 NHE6에 의한 새로운 신경전달물질 분비조절 기전
논문링크
https://www.pnas.org/content/118/2/e2011371118

