[연구동향]
Priming mobilization of hair follicle stem cells triggers permanent loss of regeneration after alkylating chemotherapy
Nat Commun. 2019
항암치료 후 발생하는 탈모는 항암 생존자들에게 심각한 문제로, 대체로 회복 가능하지만 마지막 항암치료 종료 후 6개월이상이 지났는데도 회복이 되지 않을 경우 영구탈모증으로 분류하게 된다. 모낭은 성장기와 휴지기의 모발주기를 평생 반복하는 대표적인 재생기관이다. 모낭줄기세포는 성장기의 초기에만 잠깐 증식하는, 매우 안정적인 성체줄기세포이지만 임상적으로 실제로 영구적인 탈모가 상당수 환자에서 발생하므로 모낭줄기세포 풀(pool)의 고갈 여부와 함께 실제로는 영구적이 아닐 수도 있을 것이라는 희망적인 의문이 남아있었다.
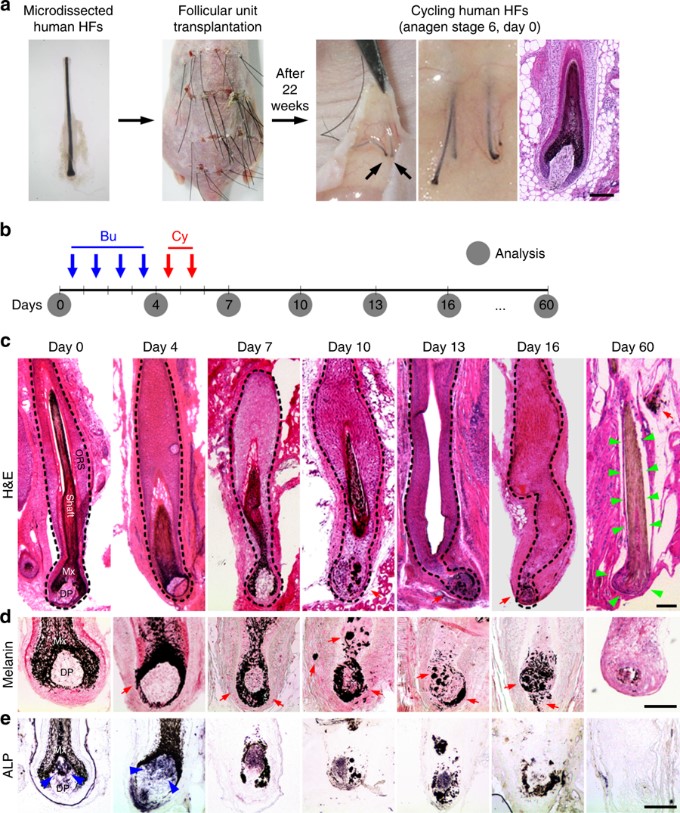
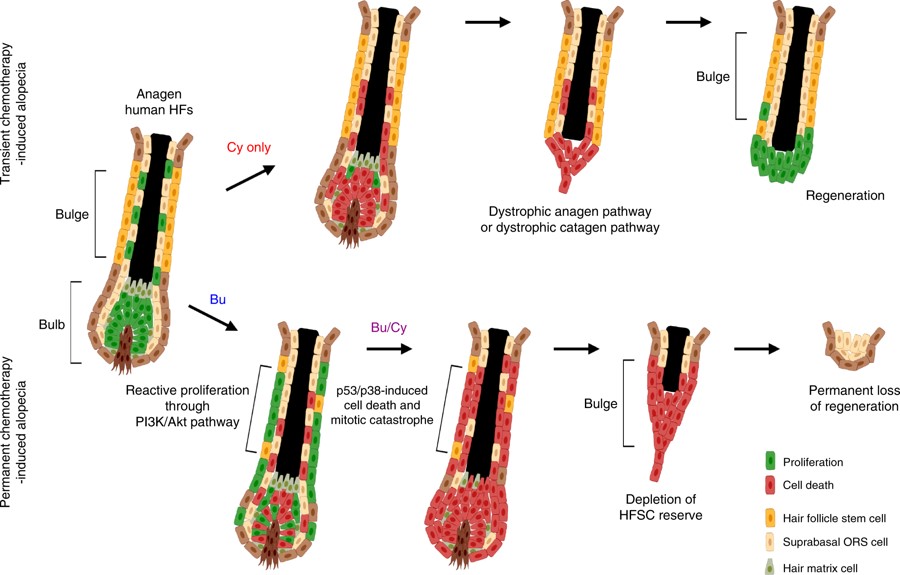
본 연구팀은 면역억제마우스에 사람의 모낭을 이식한 후, 임상환경에서 실제 사용되는 항암치료와 조혈모세포 이식스케줄을 모사하여 영구탈모 동물모델을 개발하였고 항암치료에 의한 실제 탈모발생과정과 함께 모낭줄기세포의 손상과 세포사멸 기전을 관찰할 수 있었다(그림1). 화학항암치료 스케줄에 따라 모낭에 초기 손상이 가해지면 모낭줄기세포가 조직손상의 회복을 위해 일차적으로 안정상태에서 반응성 증식(priming mobilization)이 발생하고 DNA손상에 매우 취약한 상태로 전환되는 것을 발견하였다. 이후 연속적인 항암치료제에 의해 비가역적인 DNA손상이 축적되게 되면, G2/M checkpoint 활성화에 따른 대량의 성체줄기세포 세포사멸(large-scale apoptosis)기전이 작동하게 되어 모낭줄기세포의 고갈과 함께 조직재생능력의 비가역적인 손실이 발생하는 과정을 확인할 수 있었다(그림 2). 정상조직의 조직손상(off-target effect)을 최소화할 수 있는 항암치료스케줄의 개발과 함께 모낭주기 조절을 통해 모낭줄기세포를 최대한 보호하는 보존치료법과 새로운 모낭재생 기술개발을 통해 영구탈모증을 해결해나갈 수 있을 것으로 생각된다.
Transfer of a healthy microbiota reduces amyloid and tau pathology in an Alzheimer’s disease animal model
Gut. 2019
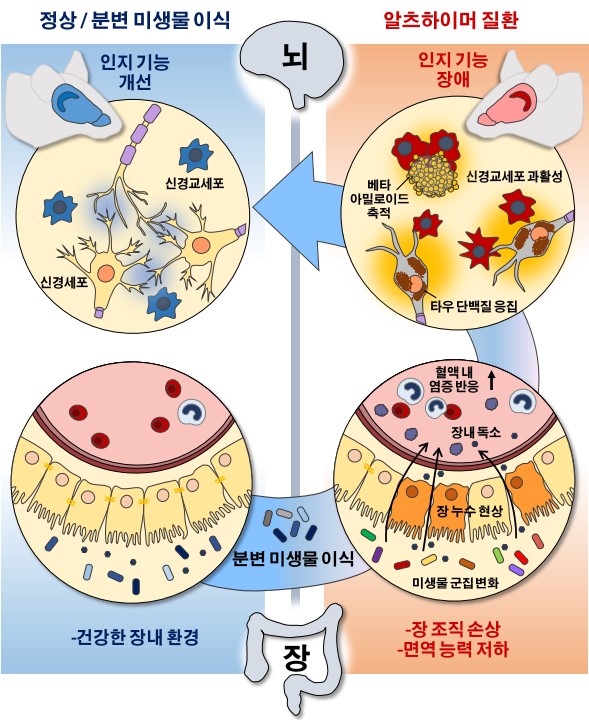
장에 공생하고 있는 미생물이 장과 뇌 간의 소통을 매개하여 뇌의 발생과정, 감정 그리고 인지기능에도 영향을 준다는 사실이 여러 정신 신경계 질환에서 밝혀졌고, 알츠하이머병 또한 영향을 받는다고 알려져 있지만 자세한 기전은 아직 명확하지 않다. 서울대학교 의과대학 생화학교실 묵인희 교수팀은 경희대학교 배진우 교수팀과 함께 장내 미생물과 알츠하이머병 증상의 연관성 및 그 기전을 새롭게 규명하고자 하였다. 장내 미생물 총의 균형이 깨진 알츠하이머성 치매 쥐를 살펴보았더니 증상이 악화될수록 장내 미생물 구성의 차이가 커졌고 이로 인해 장 누수현상과 염증반응이 일어났다. 정상 쥐의 건강한 분변을 질환 모델 마우스에 투여하는 분변 미생물군 이식(fecal microbiota transplant)을 통해 장내 환경의 변화를 유도한 결과, 기억 및 인지기능 장애가 회복되었고 뇌내 특징적인 단백질 축적과 신경세포의 염증반응이 완화되었다. 더불어 장 조직 세포의 퇴화와 혈중 염증성 면역세포 수가 정상 수준으로 회복되어 전신적인 염증 반응이 감소함을 확인하였다. 뇌 병변을 직접 표적으로 하는 치료제 개발이 난항을 겪는 가운데 이번 연구는 장내 미생물을 통한 장-뇌 축과 혈액의 면역 세포의 역할에 주목함으로써 새로운 전략의 알츠하이머병 예방 및 치료의 가능성을 제시한 것에 의의가 있다.
<논문링크>
https://gut.bmj.com/content/early/2019/08/29/gutjnl-2018-317431
Cyclase-associated protein 1 is a binding partner of proprotein convertase subtilisin/kexin type-9 and is required for the degradation of low-density lipoprotein receptors by proprotein convertase subtilisin/kexin type-9
EUR HEART J. 2019

LDL-콜레스테롤은 간에서 만들어져서 혈관을 통해 각 장기에 보급되어 원래의 역할인 세포막/호르몬 생성의 재료로써 이용된다. 그런데 혈중 수치가 높으면, 혈관벽에 침착되어서 죽상동맥경화증을 야기시키고, 심근경색증, 뇌경색증을 초래하게 된다. 혈중 LDL-콜레스테롤이 제거되는 경로는, 간에서 LDL-수용체와 결합한 뒤 간세포 내에서 분해된 후 담즙으로 소모 및 배설된다. LDL-콜레스테롤을 제거하는 데에 핵심 역할을 하는 LDL-수용체는 간세포 표면에 존재하며 LDL-수용체가 많을수록 혈중 LDL콜레스테롤 수치를 낮출 수 있다.
PCSK9 단백질이 LDL-수용체를 파괴한다는 것이 알려지면서, 이러한 현상을 억제하기 위해서, PCSK9 억제항체가 개발되어 시판되었고, LDL-콜레스테롤 강하 효과가 탁월하여 현재 전세계적으로 엄청난 판매고를 올리고 있다. PCSK9이 LDL-수용체를 파괴한다는 사실은 알려져 있지만 그 정확한 분해기전은 알려져 있지 않았다. 5년여의 연구 끝에 우리연구팀이 최초로 발견한 것은, LDL-수용체를 파괴시키는데 PCSK9 혼자만 있어서는 불가능하고, 반드시 CAP1 단백질이 있어야만 LDL-수용체를 파괴할 수 있다는 것이다. 이 연구의 가치는, 큰 성공을 거두고 있는 PCSK9 억제 항체와 경쟁할 수 있는 새로운 치료제의 개발의 문을 열었다는 것에 있다.
혈액의 LDL-콜레스테롤이 LDL-수용체와 결합하면, 클라스린이라는 세포내 유입경로를 통해서 간세포 안으로 들어와서 LDL-콜레스테롤은 분해 소모된다. 한편 LDL-수용체는 다시 세포표면으로 이동하여 재활용된다. LDL-수용체가 PCSK9 단백질과 결합하면, CAP1단백질을 통해 LDL수용체–PCSK9-CAP1단백질이 서로 결합하면서 카베올린이라는 세포내 유입경로를 통해서 들어와서 LDL-수용체가 분해되어 사라지게 된다. LDL-콜레스테롤이 현저히 낮은 사람들에게서 보고된 PCSK9유전자 변이들을 찾아서, 이들 변이 유전자를 이용하여 변이 단백질을 합성하여 분석한 결과, CAP1과의 결합에 장애가 있다는 것을 밝혔다. 즉 변이 PCSK9 단백질은 CAP1과 결합이 되지 않기에 LDL-수용체가 파괴하지 못하기에 LDL-콜레스테롤이 현저히 낮게 유지되는 기전을 밝혔다. 본 연구로써 정확한 콜레스테롤치 조절 기전을 이해하게 됨으로써 이상지질혈증과 동맥경화증 등 심혈관질환연구에 새로운 치료방향을 열게 되었다.
현재 우리 연구팀에서는 CAP1 단백질의 작용을 차단하는 선택적 억제제를 개발하고 있으며, 동물 실험에서 고지혈증과 지방간 등 대사성 질환의 증상을 완화시키는 것을 확인하고 있는 만큼, 이 기전을 응용한 신약이 조만간 가시화 될 것으로 기대한다.
CAP1이 PCSK9과 결합하여 LDL 수용체를 지질 뗏목으로 유도, 카베올린, 리소좀을 거쳐 분해시키는 과정. [좌] 혈중 LDL 콜레스테롤이 간세포표면의 LDL 수용체 (LDLR)와 결합해서 세포내로 흡수됨. 이 과정에서, PCSK9, CAP1, 카베올린 (Caveolin1)이 LDL수용체와 복합체를 형성함. 아래는 PCSK9과 CAP1의 결합부위 구조. [우] 간세포에서 LDL 콜레스테롤이 LDLR와 결합하면 둘 중 하나의 흡수과정을 겪게 됨. 즉, PCSK9, CAP1, Caveolin1과 결합하면 지질뗏목으로 유도되어 카베올라 소낭, 엔도솜을 거쳐 리소좀에서 LDL수용체가 분해됨. 반면 CAP1의 결합이 없을 경우에는 LDL-C / LDL-R 결합체는 클라스린-피복 소낭을 거쳐 재순환 사이클로 유도되어 LDL-C는 세포내에서 분해 사용되고, LDL 수용체는 세포막으로 돌아가서 재활용 됨.
<논문링크>
https://academic.oup.com/eurheartj/advance-article/doi/10.1093/eurheartj/ehz566/5550816
Intensive care unit length of stay is reduced by protocolized family support intervention: a systematic review and meta-analysis
INTENS CARE MED. 2019
대부분의 중환자실 환자들은 본인의 치료에 관한 중요한 의사 결정 과정에 직접 참여하지 못하고 환자의 가족들이 대신하는 경우가 많기 때문에, 가족들은 이 과정에서 상당한 심적 부담감을 느끼게 된다. 특히 중환자실 의료진과의 의사소통이 원활치 않아 충분한 정보를 제공받지 못했다고 느낄 경우, 우울증, 불안장애와 같은 여러 가지 신경정신학적 문제들의 발병 위험이 상승하는 것으로 알려져 있다. 따라서 의료진과 환자 가족 간의 의사소통을 향상시키기 위해, 여러 가지 중재법을 연구하고 있고, 그간의 대부분의 연구들은 주결과변수(primary outcome)로 ‘보호자의 의사결정과정에 대한 만족도’ 혹은 ‘환자 사망 이후 3~6개월째 보호자들의 신경정신학적 증상의 유무’를 보았다. 그러나, 본 연구진은 의료진과 가족 사이에 원활한 의사소통이 이루어진다면, 중환자실에서 가장 중요한 치료의 목적(goals of care)을 초기에 정립하고, 그에 따른 합리적 의사결정이 적절한 시점에 이루어져 불필요한 연명의료를 줄여, 궁극적으로 중환자실 재원기간을 줄일 수 있을 것으로 생각하였다. 다만, 이러한 중재는 사전에 잘 구축된 프로토콜이 있고, 중재는 철저하게 그 프로토콜에 따른 가족 미팅이어야 효과가 있을 것으로 전제하였다.
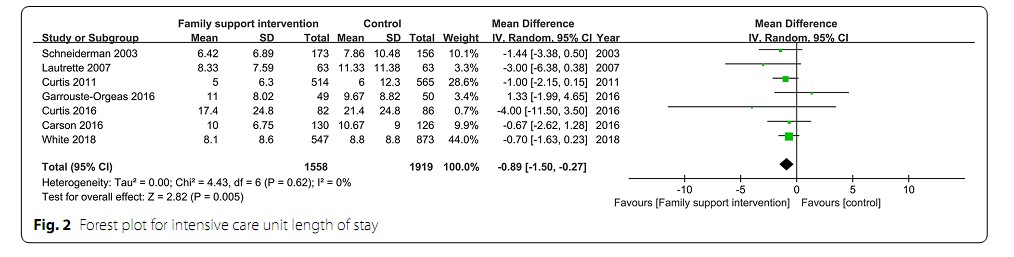
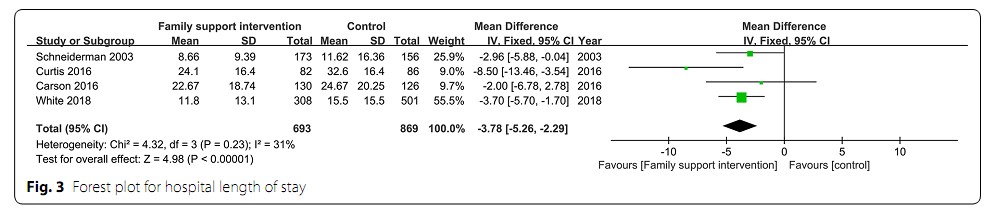
이에 중환자실 재원기간을 주결과변수로 하여, 중환자실 환자 가족들의 지지적 중재에 대한 7개의 무작위 배정 비교-대조군 연구를 메타분석 하였다. 총 3477명의 환자에서 중재군은 대조군에 비해 중환자실 재원기간을 0.9일, 병원 총재원기간을 3.8일 감소시켜주는 것으로 나타났다. 또한 서브그룹 분석을 통해 특히 증상완화(comfort care)목적의 환자군에서, 중환자실 입실 초기(72시간 이내)에 이런 중재를 했을 때 그 효과가 유의하다는 것을 밝혀냈다.
이 연구는 중환자실 가족들에 대한 다양한 중재의 종류를 “구체화된 프로토콜이 존재하는 가족미팅(protocolized family meeting)”으로 한정했다는 점과 함께, 중환자실 재원기간을 주요 결과변수로 본 첫 번째 연구라는 점, 또한 high quality RCT만을 메타 분석에 포함하여 연구 결과에 대한 근거 수준이 매우 높다는 점에서 그 의미가 있다.
<논문링크>
https://link.springer.com/article/10.1007%2Fs00134-019-05681-3
Overproduction of inter-α-trypsin inhibitor heavy chain 1 after loss of Gα13 in liver exacerbates systemic insulin resistance in mice.
Sci Transl Med. 2019
우리 몸의 간은 대사적 스트레스에 반응하여 여러 가지 분비 단백을 생성하고 유리한다. 정상 대조군에 비해 당뇨병 생쥐와 환자의 간에서 Gα13 유전자의 선택적 발현 감소를 관찰할 수 있었다. Secretome 분석 결과, 인슐린 저항성 및 고혈당과 관련하여 간에서 다량으로 분비하는 특정 단백 (inter-α-trypsin inhibitor heavy chain 1, ITIH1)을 확인할 수 있었다. 혈중 ITIH1의 당화 변형은 지방조직과 골격근조직 주위의 히알루론산에 ITIH1의 침착을 촉진하고 인슐린과 인슐린 수용체 사이의 물리적 장벽으로 기능한다. 분비된 ITIH1에 대한 중화항체 치료는 전신 인슐린 저항성을 개선시키고 당불내성을 호전시켰다. 본 연구 결과는 각종 대사질환(당뇨, 지방간, 심혈관질환 등)을 치료하기 위한 새로운 치료적 전략을 개발하는데 있어 중요한 기초 개념을 제공한다는 의의를 갖는다.


