[연구동향]
Tocilizumab treatment for new-onset refractory status epilepticus.
Ann. Neurol.2018

이상건, 주건, 이순태 교수(신경과학교실), 전진선 전임의 (현 칠곡경북대학교병원 교수)
난치성경련중첩증(New-onset Status epilepticus, NORSE)은 건강하던 사람이 갑자기 경련 발작을 시작하여 항경련제를 투약하여도 멈추지 않는 상태를 말하는데, 응급질환이면서도 극도의 중증 난치성 신경 질환이다. 현재까지는 뚜렷하게 효과가 있는 단일 치료제는 없는 실정으로, 항경련제를 초고용량으로 증량해서 사용하면서 전신마취, 기본적인 면역억제제 치료를 하는 것이 제한된 방법이었다.
그런데 본 연구진은 난치성경련중첩증이 자가면역질환이거나, 아니면 경련이 멈추지 않는 현상자체에 염증매개물질이 중요하게 작동할 것으로 가설하고, 환자의 뇌척수액 분석을 통해 IL-6 사이토카인이 주요 마커임을 확인하였다. 이에 IL-6 수용체 억제제인 토실리주맙(Tocilizumab) 을 투약하였으며, 연속적인 7명의 시도에서 6명이 난치성경련중첩증이 멈추는 효과를 확인하였다. 현재까지 난치성경련중첩증 치료효과로서는 가장 우수한 결과로서, 신경과학 분야에서는 가장 우수한 저널중 하나인 Annals of Neurology에 출간되었다. 향후 난치성경련중첩증 환자에서 효과적인 치료 옵션이 될 수 있겠으며 지속적인 전향적 연구와 분석을 통해 효용과 안전성 데이터를 마련해갈 계획이다.
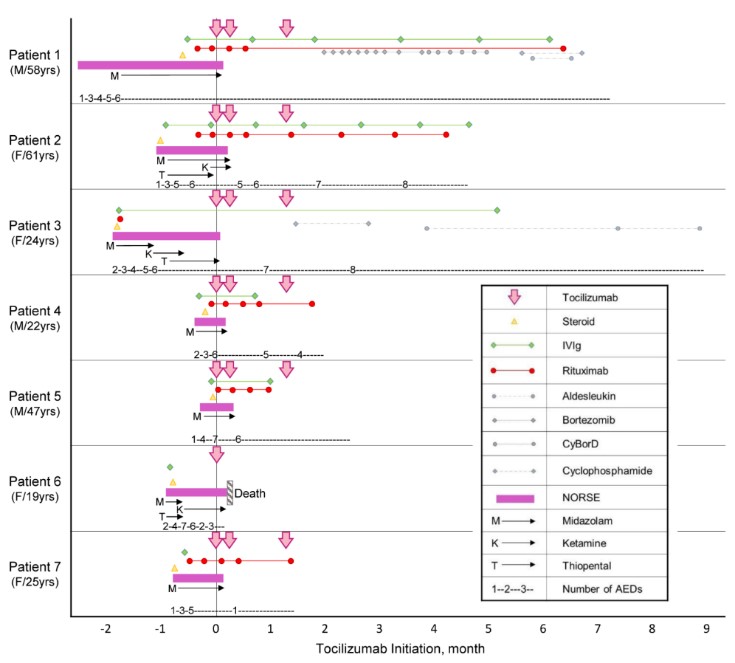
그림. 난치성경련중첩증 환자 7명의 치료내역와 토실지주맙치료성적
Innate immune crosstalk in asthmatic airways: innate lymphoid cells coordinate the polarization of lung macrophage
J Allergy Clin Immunol. November 2018
강혜련 교수(내과학교실), 김혜영 교수(의과학과), 김지현(대학원생)
천식은 기도 내 다양한 면역세포의 상호작용에 의해 발생하는 만성 염증질환이다. 지금까지의 천식에 관한 연구는 Th2 세포에 의해 항원 특이적으로 유도되는 알러지성 천식에 주로 초점이 맞추어져 있다. 하지만 최근 환경적 요인이나 바이러스 감염, 스트레스, 비만 등의 다양한 요인에 의해 발생하는 비알러지성 천식의 중요성이 대두되고 있다. 비교적 최근 밝혀진 면역세포인 선천성림프구세포는 점막에 주로 존재하며 다양한 자극에 의해 빠르게 반응하는 선천면역세포이다. 본 연구팀에서는 동물 모델을 사용하여 선천성림프구세포가 천식의 발병기전에서 중요한 역할을 수행할 수 있다는 사실을 연구해왔지만 실제 천식 환자에서 선천성림프구세포가 어떻게 변화하고 다른 면역세포와 어떻게 상호작용 하는지에 대해서는 잘 알려져 있지 않았기 때문에, 다양한 천식 환자군에서 선천성림프구세포가 어떠한 기능을 담당할 수 있는지에 대한 연구를 진행하였다.
본 연구에서는 천식환자에서 선천성림프구세포가 대식세포의 분화 및 기능을 조절함으로써 천식의 발병 및 알러지성 혹은 비알러지성 천식에 관여되어 있음을 규명하였다 (그림1). 알러지성 천식에서는 type2 사이토카인을 분비하는 선천성림프구세포가 대식세포를 M2형으로 분화시켜 알러지 반응을 강화시키고, 비알러지성 천식에서는 type3 사이토카인을 분비하는 선천성림프구세포와 M1 대식세포의 상호작용을 통해 질환이 조절될 가능성을 제시하였다. 본 연구를 통해 천식의 특정상황에서 활성화될 수 있는 세포의 종류가 다름을 확인하였고, 천식의 발병 기전을 세분화함으로서 환자의 특성에 맞는 치료의 필요성을 제시하였다.
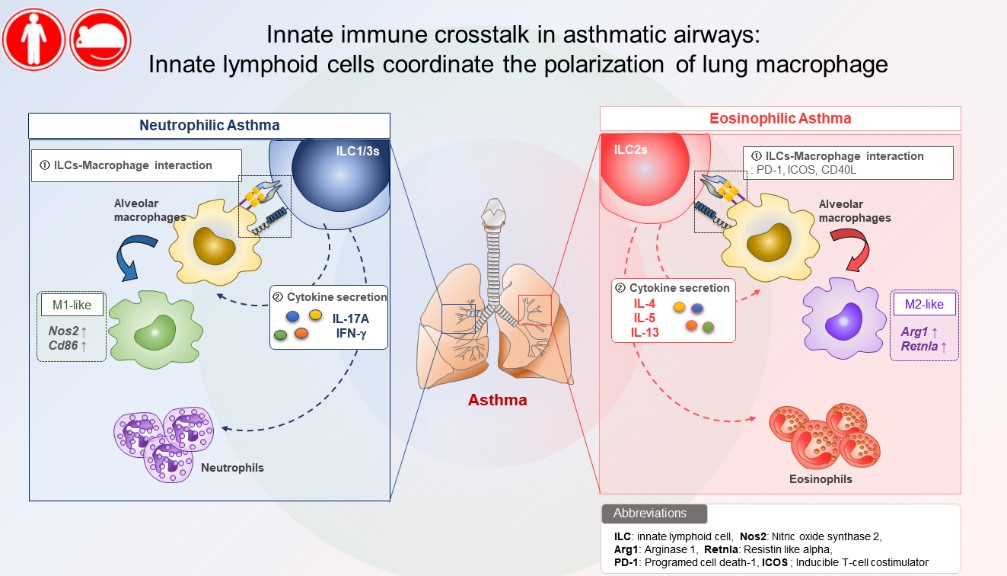
그림. 천식환자에서 선천성림프구세포와 선천면역세포의 상호작용
https://www.sciencedirect.com/science/article/pii/S0091674918315823
The Effect of a Smartphone-Based, Patient-Centered Diabetes Care System in Patients With Type 2 Diabetes: A Randomized, Controlled Trial for 24 Weeks.
Diabetes Care, 2018

조영민 교수(내과학교실)
당뇨병은 대표적인 만성질환으로 매일매일 환자 본인이 식이요법, 운동요법, 혈당측정, 약 복용, 인슐린 주사 등을 해야 한다. 그러나 정작 의료진과 만나서 상담하는 시간은 매우 짧아서, 우리나라의 현실을 감안할 때 1년에 채 15분이 되지 않는 경우가 많다. 이런 문제점을 해결하기 위해서 서울대학교 병원 내분비내과 연구진은 서울대병원/SK 텔레콤이 공동설립한 헬스커넥트와 함께 당뇨병 관리용 앱을 개발하였다.
이 앱의 특징은 당뇨병 환자를 치료 형태에 따라 네 개의 그룹으로 나누어 개별화를 도모했고, 행동과학 이론에 입각한 식이요법, 운동요법 모듈을 만들었으며, 혈당 측정 및 운동량 모니터링이 블루투스를 이용해 자동으로 입력되도록 했으며, 혈당 측정 결과 등에 대해 CDSS (임상결정보조시스템)를 통해 즉각 피드백이 가도록 했고, 인슐린 용량 결정 알고리듬을 탑재하여 혈당 측정 결과에 따라 적절한 인슐린 용량을 추천한다는 점이다. 서울대병원, 분당서울대병원, 보라매병원이 참여하여 24주간 효과를 관찰했을 때 0.4% 정도의 당화혈색소 감소가 유의하게 관찰되었으며, 특히 연구 참여 시점의 당화혈색소가 높거나, 인슐린을 사용하는 사람에서는 더 효과가 컸다. 본 앱은 일부 기능을 편집하여 무료로 배포 예정이며, 해외에서 사업화가 준비 중에 있다.
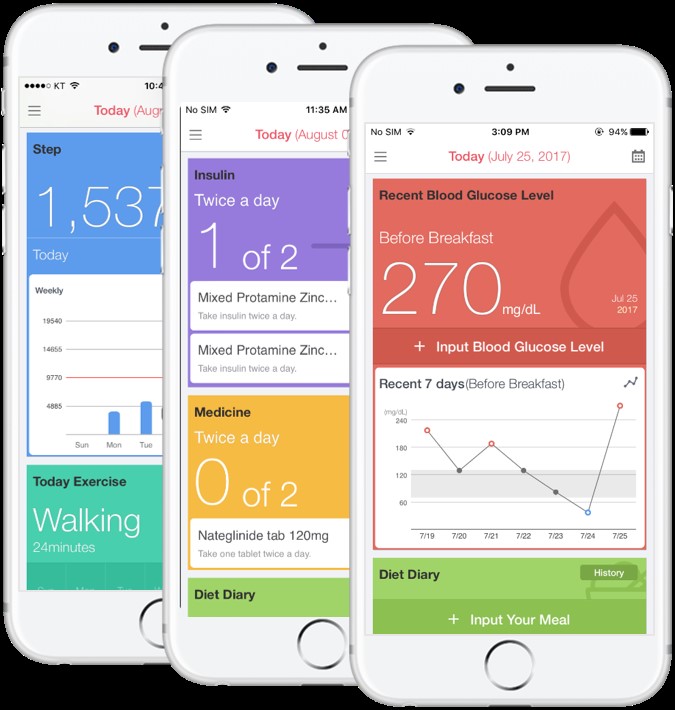
http://care.diabetesjournals.org/content/early/2018/11/05/dc17-2197
Non-invasive response prediction in prophylactic carvedilol therapy for cirrhotic patients with esophageal varices
J Hepatol. 2018

김원 교수(내과학교실, 보라매병원)
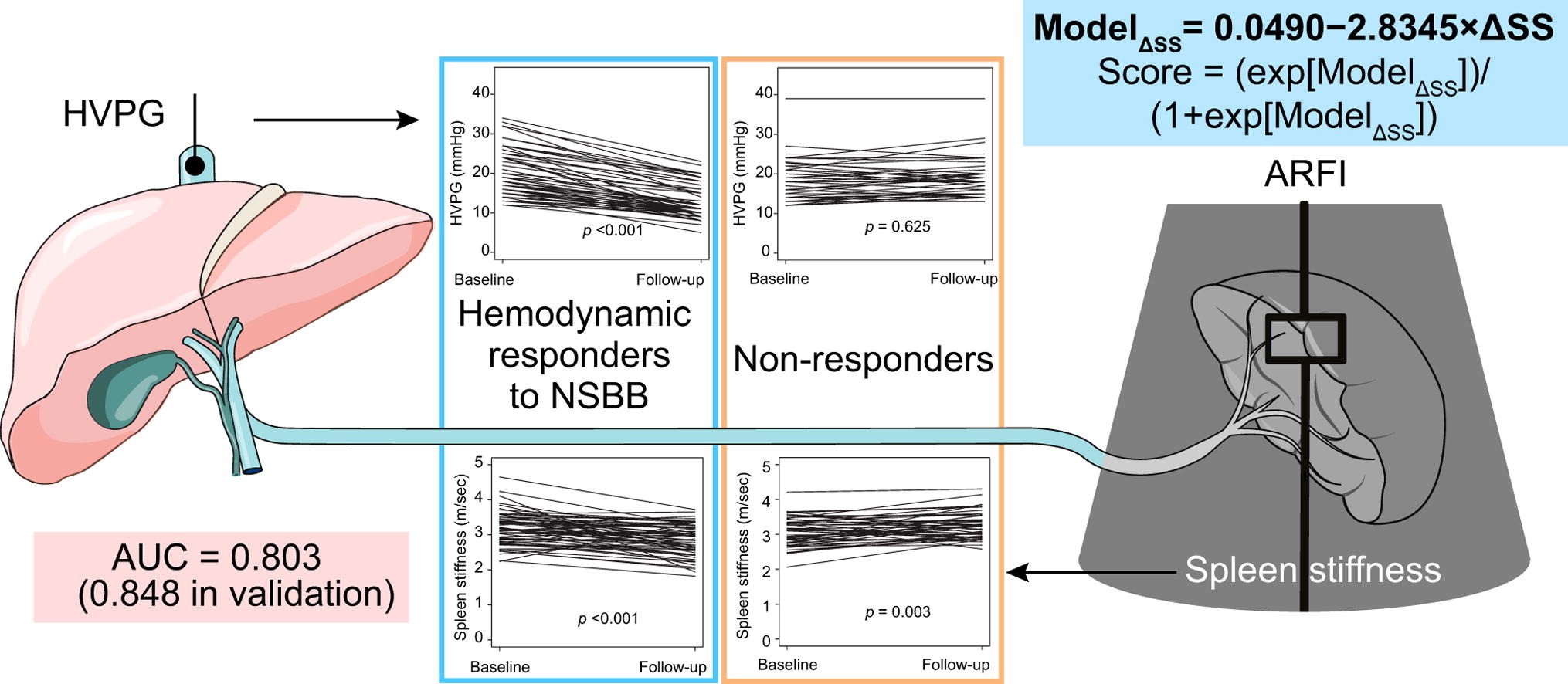
비선택적 베타차단제는 출혈의 고위험 식도 정맥류를 갖는 간경변 환자들에서 정맥류 출혈을 예방하기 위한 일차 예방 치료의 근간이 된다. 보라매병원에서는 세계 최초로 단일 기관 전향 코호트 연구를 통해 약물 투여 전후의 비장 탄성도의 변화에 기반한 혈역학적 예측 모형을 통해 간문맥압 감소 여부를 비침습적으로 정확하게 예측할 수 있었다 (그림 1).
본 연구를 통해 지금까지 시행해온 간문맥-정맥압 경사차 측정을 위한 침습적이고 고비용인 혈관조영술을 피하면서도 간단하게 탄성초음파 검사만으로도 손쉽게 간문맥압 측정을 대신할 수 있었고 간문맥압 항진증에서 일반적으로 사용되는 베타 차단제에 대한 혈역학적 반응 여부를 매우 정확하게 예측할 수 있었다. 향후 본 연구 결과를 통해 식도 정맥류가 있는 간경변 환자에서 침습적인 혈관조영술을 시행하지 않고도 고위험군의 선별과 치료 반응의 조기 예측이 가능하게 되어 치료 무반응군으로 예상되는 환자군에서는 조기에 베타 차단제를 중단하고 내시경적 식도정맥류 결찰술을 시행할 수 있는 근거를 마련했다는 측면에서 큰 의의가 있다.
https://www.sciencedirect.com/science/article/pii/S0168827818325029
Association of Blood Pressure Classification in Korean Young Adults According to the 2017 American College of Cardiology/American Heart Association Guidelines With Subsequent Cardiovascular Disease Events
JAMA. 2018.

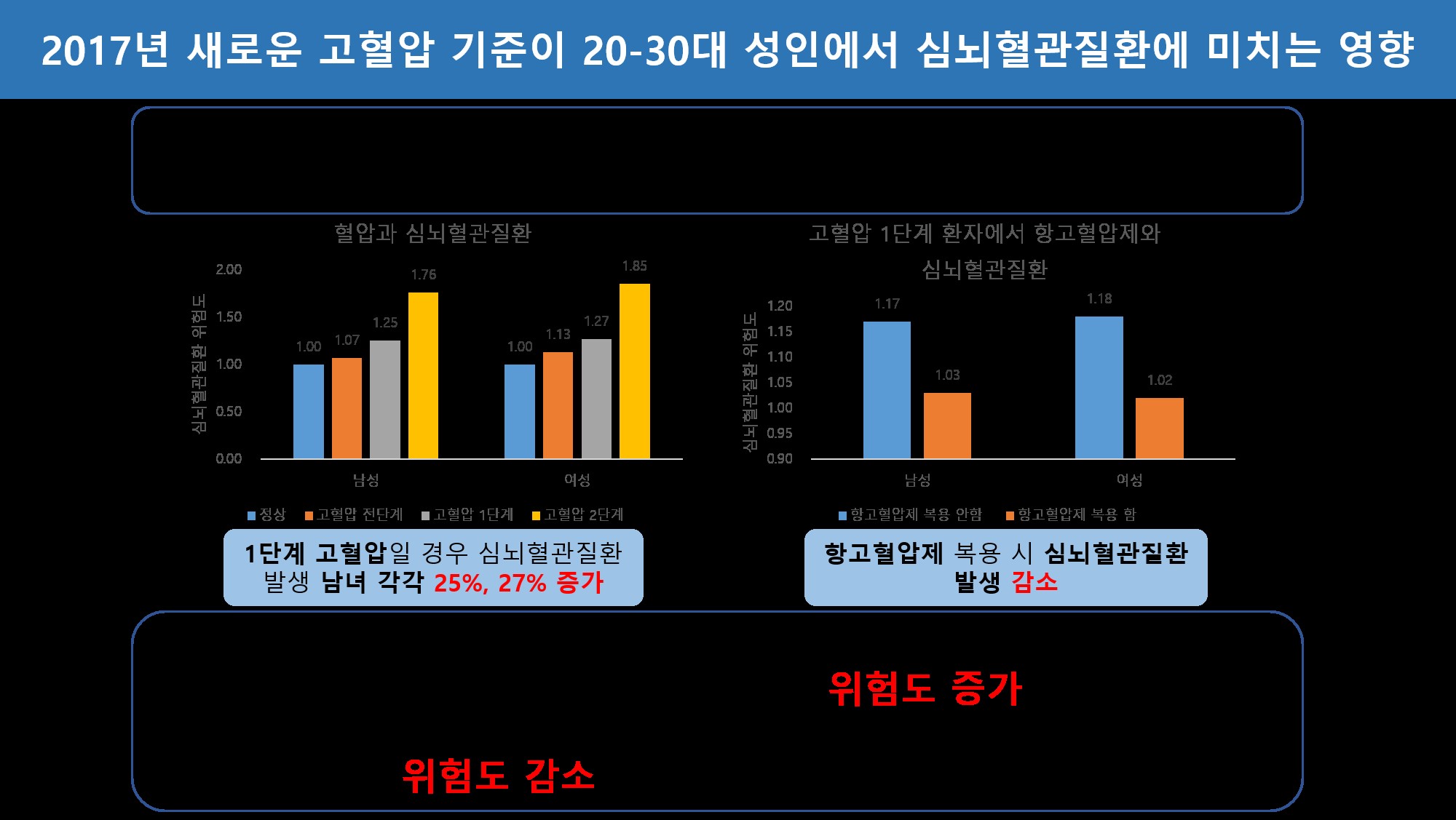
2017년에 미국심장학회(ACC) 및 미국심장협회(AHA)에서 기존의 고혈압 기준인 140/90 mmHg 보다 더 낮은 130/80 mmHg 이상을 새로운 고혈압 기준으로 정의하였다. 2017년 새로운 기준에 따르면, 정상 혈압은 120/80 mmHg 미만, 상승 혈압(Elevated BP)은 120~129 mmHg 및 80 mmHg 미만, 1단계 고혈압은 130~139 mmHg 또는 80~89 mmHg, 그리고 2단계 고혈압은 140/90 mmHg 이상이다.
최근 다양한 연구들에서 40세 이상 중장년층에서 혈압이 130/80 mmHg만 되어도 심뇌혈관질환 발생 위험도가 증가한다는 결과들을 바탕으로 새로운 고혈압 기준이 생겼다. 그러나, 새로운 고혈압 기준이 20~30대 젊은 성인에서도 높은 심뇌혈관질환 발생 위험도와 연관이 있는지에 대해서는 자세히 알려지지 않았다.
최근 서울대학교병원 가정의학과 박상민 교수 연구팀(공동 제1저자 손정식 교수, 최슬기 연구원)은 20~30대 성인에서 혈압과 심뇌혈관질환 발생의 연관성을 연구하였다. 국민건강보험공단의 빅데이터를 활용하여 2002년~2003년과 2004년~2005년 2회 건강검진을 받은 20~30대 남녀 2,488,101명을 대상으로 10년간 추적 관찰한 연구결과, 새로운 고혈압 기준으로 1단계 고혈압일 경우에도 심뇌혈관질환 발생 위험이 증가하고, 고혈압인 사람이 항고혈압제를 복용할 경우 심뇌혈관질환 발생 위험이 낮았다는 결과가 나왔다.
정상 혈압인 사람에 비해 1단계 고혈압인 20~30대 젊은 성인에서 심뇌혈관질환 발생 위험도가 남녀 각각 25% 및 27% 증가하였다. 또한, 고혈압에 있는 20~30대 젊은 성인이 항고혈압제를 복용할 경우 심뇌혈관질환 발생 위험도가 낮았다. 이번 연구에서 20~30대 젊은 연령대 성인 남녀에서 2017년 새로운 기준의 고혈압이 심뇌혈관질환 발생 위험도를 높이는 것을 밝혔으며, 20~30대 젊은 연령대부터 심뇌혈관질환 예방을 위해 혈압 관리의 중요성을 확인 할 수 있었다.
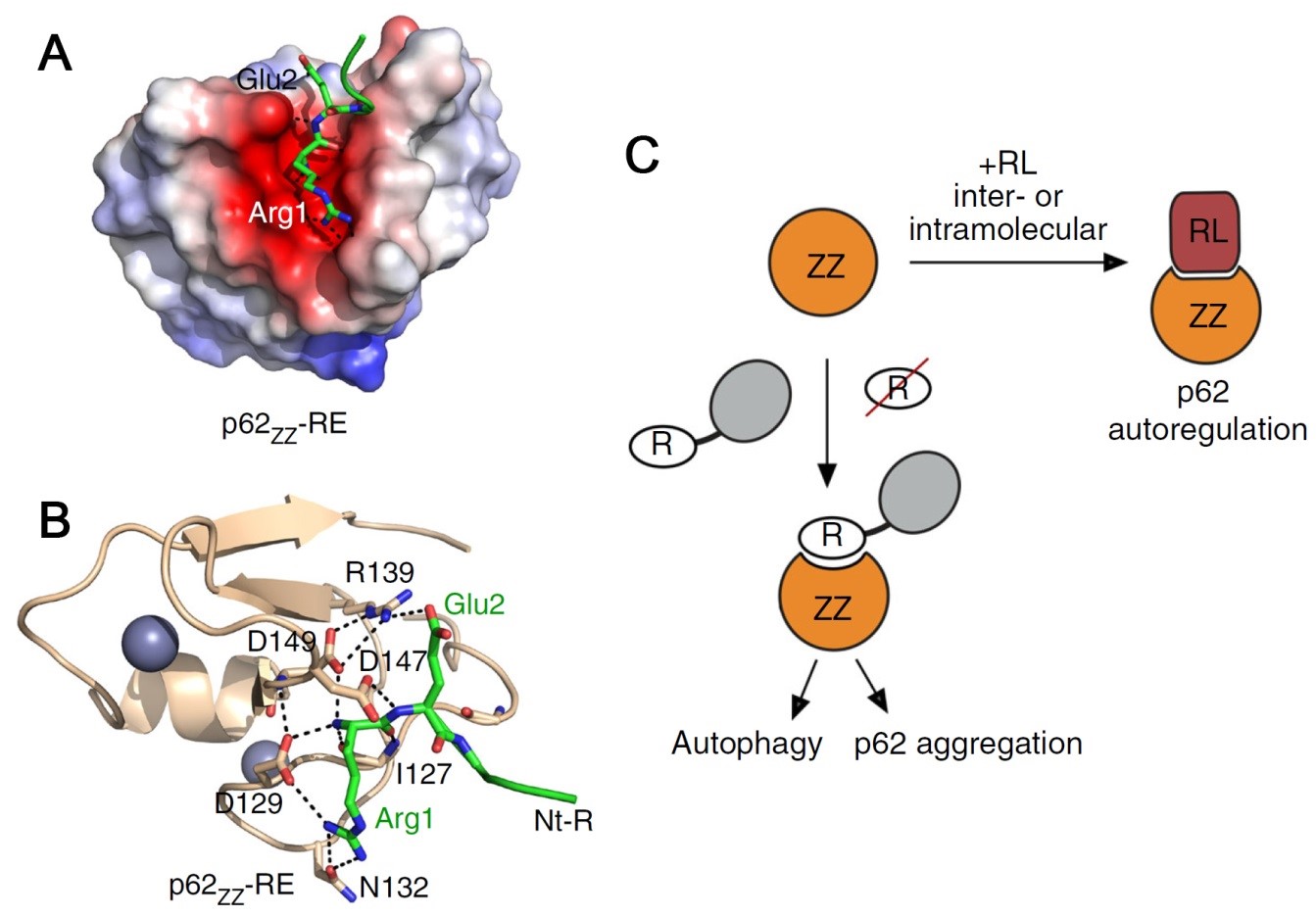
ZZ-dependent regulation of p62/SQSTM1 in autophagy
Nature Comm., 2018

생체 내 존재하는 단백질들은 매일 6%가 분해되고 새로 합성된다. 단백질 항상성을 유지하기 위해서 전체 유전자의 약 10%에 해당하는 단백질들이 네트워크를 이루어 작용하며, 이들 대부분은 유비퀴틴-프로테아좀 시스템(ubiquitin-proteasome system) 및 오토파지(autophagy) 시스템에 속한다. 단백질이 변성되거나 응고체를 형성하는 경우 유비퀴틴 프로테아좀 시스템, 오토파지 등에 의하여 분해되지만, 단백질 항상성은 세포의 스트레스와 노화 과정에서 끊임없이 도전을 받기 때문에 기능이 저하되거나 손상될 수 있다. 이로 인한 비정상적인 단백질의 축적과 침전은 암, 퇴행성 뇌질환(알츠하이머성 치매, 파킨슨병, 헌팅턴병, ALS, 광우병 등), 당뇨로 대표되는 대사질환, 감염/면역질환, 황반변성으로 대표되는 안과질환, 알코올성 간경화, 1-antitrypsin deficiency나 cystic fibrosis를 포함하는 각종 효소결핍증 등 매우 다양한 질환의 병인이 되고 있다. 현재로선 이들 변성단백질을 뇌 등 인간의 신체 조직에서 선별적으로 제거하는 방법이나 치료제는 전무하며, 의학계의 큰 숙제 중의 하나이다.
본 연구실에서는 노화 과정에서 관련 질병 유발 변성 단백질의 분해기작과 제어기술을 연구하고 있으며, 선행연구에서 오토파지 리셉터인 p62가 N-말단 분해경로의 리간드에 의해서 조절된다는 사실을 밝힌 바 있다. 본 연구에서는(18’ Nature Communications) 미국의 콜로라도 대학의 단백질구조 연구실과의 공동연구를 통하여, p62의 ZZ 도메인의 구조를 밝히고, N-말단 리간드가 어떻게 p62 ZZ 도메인에 결합하여 p62의 활성 및 오토파지 흐름을 조절하는지 그 분자생물학적인 기작을 규명하였다. 본 연구를 통해서, 오토파지 조절을 이용한 질병 치료 연구가 더 가속화될 것으로 예상된다.