[연구동향]
Cerebellar Bergmann glia integrate noxious information and modulate nocifensive behaviors
Nature Neuroscience

(생리학교실,공동교신저자)

(의과학과,공동제1저자,
현 UTSW)

(의과학과,공동제1저자)
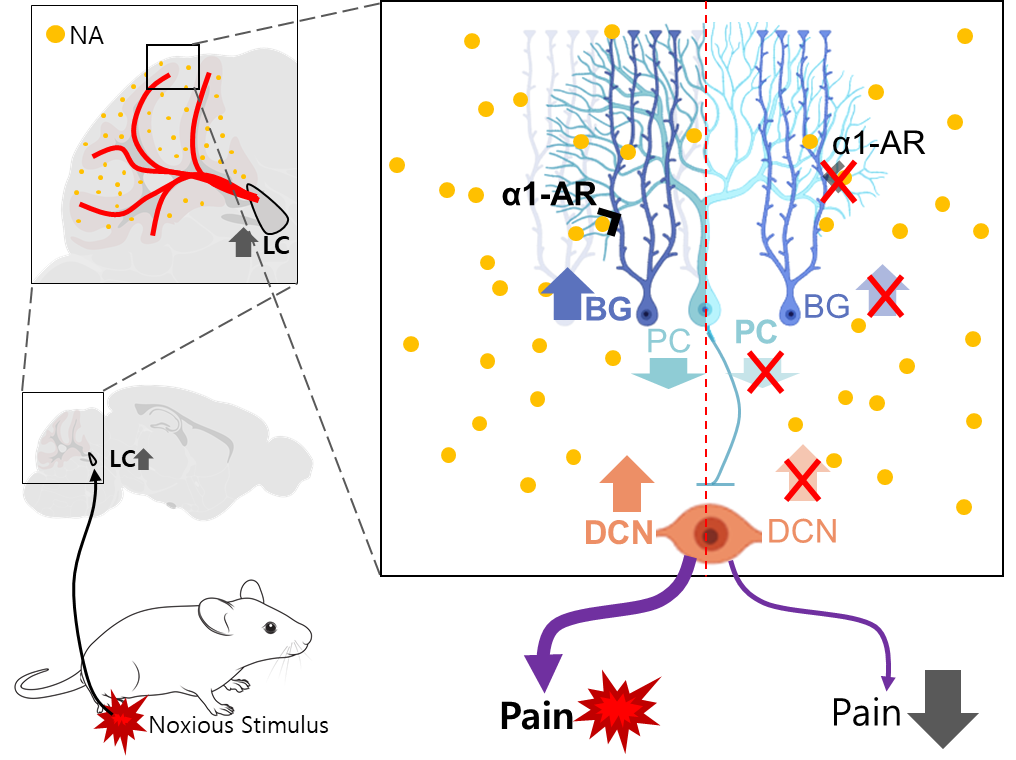
서울대학교 의과대학 생리학교실 김상정 교수 연구팀은 소뇌가 통증 정보를 처리하고 통증 행동을 조절하는 기전을 밝혔다. 연구팀은 전기생리학, 광유전학, 2광자 이미징 등을 활용해 소뇌의 버그만 글리아(Bergmann glia, BG)가 노르아드레날린(noradrenaline, NA)을 통해 유해 자극 정보를 통합하고 통증 행동을 조절하는 과정을 분석했다.
연구 결과 유해 자극은 청색반점(locus coeruleus, LC)에서 NA를 방출시켜 소뇌 버그만 글리아의 칼슘 신호를 활성화시키며 이는 퍼킨지 세포(Purkinje cell)의 발화율 감소를 유도했다. 이 과정은 소뇌 심부핵(deep cerebellar nuclei)의 활동을 조절해 통증 행동에 영향을 미쳤다. 특히, NA 수용체(α1-아드레날린 수용체)를 차단하거나 BG 칼슘 신호를 억제하면 통증 행동이 감소했다.
이번 연구는 소뇌가 단순히 운동 조절뿐 아니라 통증 정보 처리에 중요한 역할을 한다는 점을 입증했으며, PTSD와 같은 스트레스 관련 질환 및 만성 통증 치료에 새로운 접근법을 제시했다.
Esophageal ILC2s mediate abnormal epithelial remodeling in eosinophilic esophagitis via Areg-EGFR signaling
Cellular & Molecular Immunology

(의과학과,교신저자)

(의과학과,제1저자)
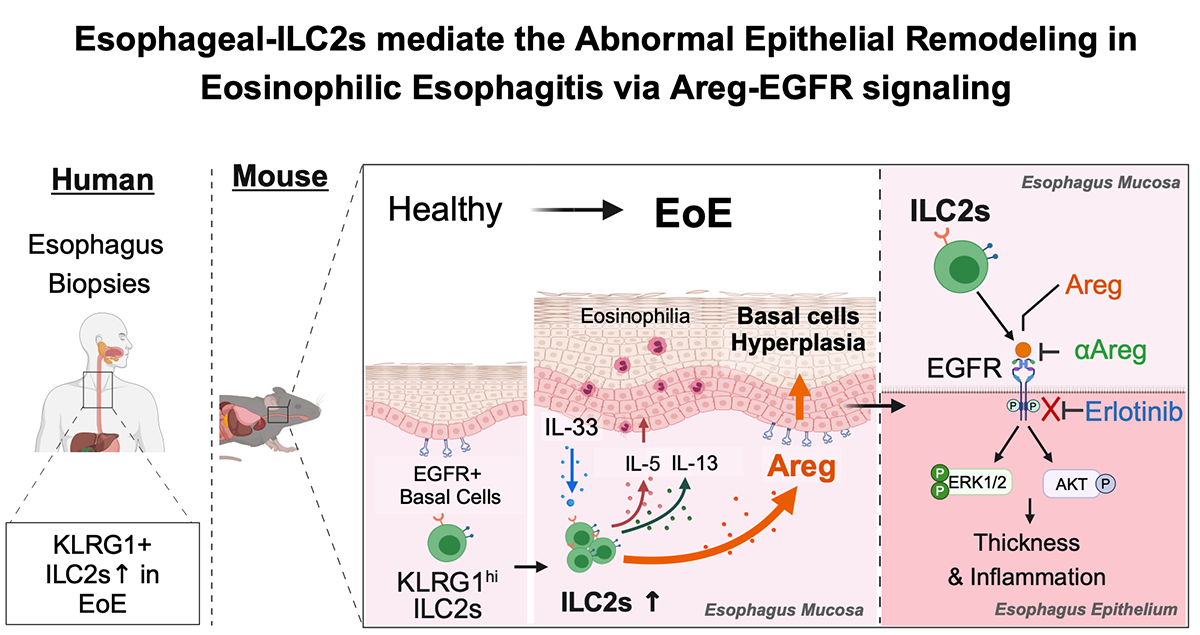
호산구성 식도염(eosinophilic esophagitis, EoE)은 식도에 만성적으로 염증이 생기고, 식도 상피세포가 과도하게 증식해 주로 음식을 삼키기 어려운 증상(연하곤란)을 유발하는 알레르기성 질환이다. 지금까지 연구에서 EoE 환자에게서 제2형 선천성 림프구세포(ILC2)의 수가 증가하고, IL-33이라는 염증 신호가 활성화된다는 사실이 밝혀졌으나, ILC2가 정확히 어떻게 식도 상피 변화에 관여하는지는 잘 알려지지 않았다.
본 연구진은 EoE 발생 과정에서 ILC2가 Amphiregulin (Areg)-EGFR 신호 경로를 활성화해 식도 상피를 비정상적으로 증식시키고 두껍게 만든다는 새로운 기전을 규명했다. 연구팀은 정상 생쥐의 식도에서는 KLRG1+ ILC2가 적은 수로 존재하지만, EoE 환자 검체와 IL-33을 주입해 만든 EoE 동물 모델에서는 ILC2 수와 ILC2에서 Areg 발현이 크게 증가한다는 점을 확인했다. Areg은 식도 상피세포 및 줄기세포의 EGFR (상피세포 성장인자 수용체)을 활성화시켜 세포 증식을 유도하고 식도 상피를 두껍게 만드는 역할을 한다는 것도 밝혀냈다. 또한 인체 식도 상피세포(CP-A, HET-1A)를 이용한 실험에서 Areg이 EGFR을 활성화해 ERK와 AKT라는 신호 경로를 자극해 상피세포 증식을 촉진한다는 사실을 확인했다. 더 나아가 동물 모델과 식도 상피세포 실험에서 Areg 중화항체나 EGFR 억제제(erlotinib)를 처리하자 식도 상피 두꺼워짐, 호산구 침윤, 염증 반응 등 EoE 증상이 뚜렷하게 완화됐다. 또한 ILC2가 결핍된 생쥐에서는 EoE 증상이 거의 나타나지 않았다.
본 연구는 EoE에서 ILC2-Areg-EGFR 신호 경로가 병을 일으키는 핵심 역할을 한다는 것을 새롭게 밝혀내어, 점막 면역 및 알레르기 염증 질환 연구에 중요한 기여를 하였다. 특히 기존 치료에 잘 반응하지 않는 난치성 EoE 환자들에게 Areg 중화항체나 EGFR 억제제를 활용한 표적 치료가 새로운 대안이 될 수 있음을 보여줬다.
AI model using CT-based imaging biomarkers to predict hepatocellular carcinoma in patients with chronic hepatitis B
Journal of Hepatology

(의학과,교신저자)

(서울대학교병원 소화기내과,
공동제1저자)

(서울대학교병원 소화기내과,
공동제1저자)
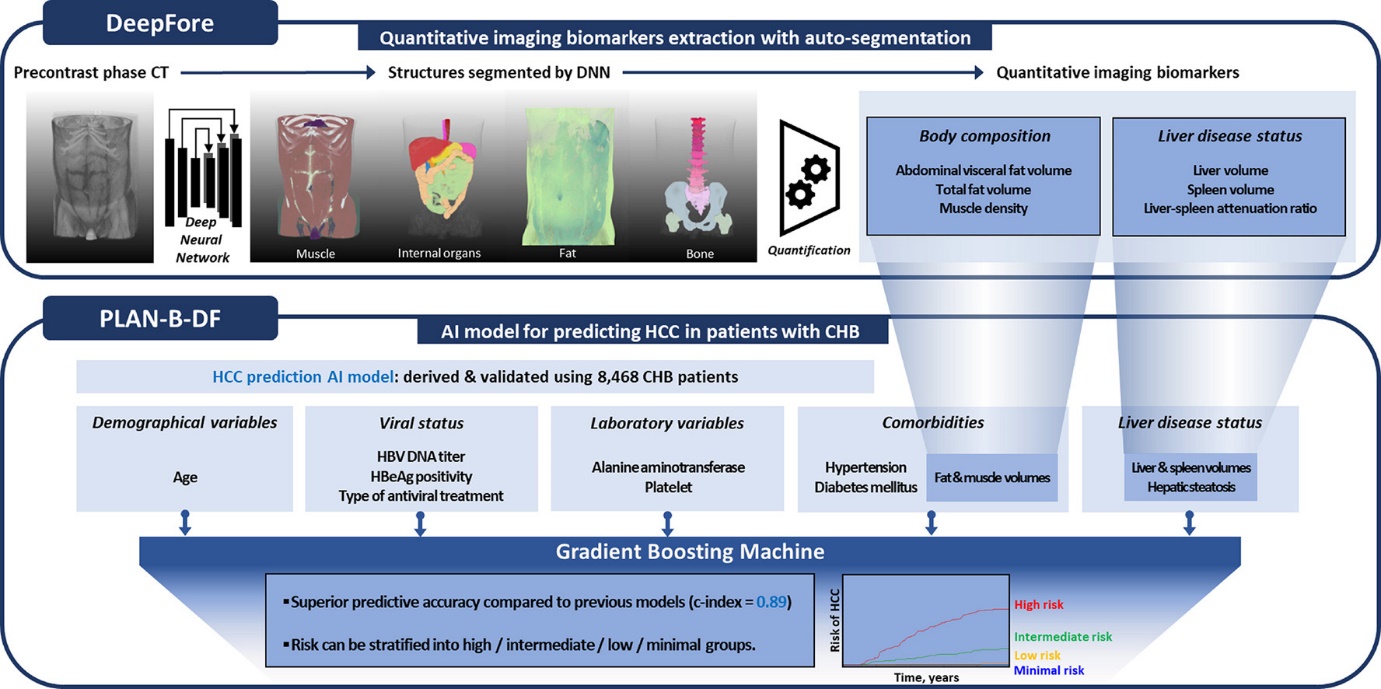
만성 B형간염 환자는 바이러스 간염 상태, 간 섬유화 정도, 기저 질환 등 다양한 요인에 의해 간암 발생 위험이 영향을 받는다. 이에 따라 유럽간학회 가이드라인에서는 PAGE-B 등의 간암 예측 모델을 기반으로 감시 전략을 수립할 것을 권고하고 있다. 그러나 기존 예측 모델들은 주로 임상 변수에 의존하며, 최근 중요성이 부각되고 있는 복부 지방량, 근육량, 근육 지방화 등과 같은 대사 및 체성분 요인을 충분히 반영하지 못하는 한계가 있다. 이에 본 연구에서는 이러한 다양한 위험 요인을 총체적으로 고려한 간암 발생 예측 모델을 개발하기 위해, 국내 대규모 다기관 코호트를 구축하고 인공지능 소프트웨어 개발 회사와 협업해 복부 CT에서 주요 지표를 자동 분할해 영상 바이오마커를 추출하는 소프트웨어를 활용했다. 이를 기반으로 간암 발생 위험도를 예측하는 인공지능 모델을 개발하고 그 성능을 검증하고자 했다.
본 연구진은 국내 5개 3차 의료기관에서 총 5,585명의 만성 B형간염 환자로 구성된 다기관 코호트를 구축해 모델 개발을 진행했다. 기계 학습 모델은 gradient boosting machine (GBM) 알고리즘을 기반으로 개발됐으며, 모델 학습을 위해 데이터를 무작위로 3:1 비율로 각각 훈련 코호트(4,188명)와 내부 검증 코호트(1,397명)로 배정했다. 이후 독립적인 모델 성능 검증을 위해 국내 2개 3차 의료기관에서 2,883명의 외부 검증 코호트를 추가로 구축했으며, 이를 활용해 모델의 예측 성능을 평가했다.
인공지능 예측 모델의 입력 변수는 총 14개로, CT 영상에서 자동 추출된 6개의 영상 바이오마커(간 부피, 비장 부피, 복부 내장 지방-총 지방 비율, 총 지방-몸통 부피 비율, 간-비장 Hounsfield Unit (HU) 비율, 근육 HU)와 8개의 임상 변수(나이, 혈소판 수치, 혈중 B형간염 DNA 수치, B형간염 e항원(HBeAg) 상태, ALT 수치, 항바이러스제 종류(entecavir 또는 tenofovir), 당뇨병 유무, 고혈압 유무)로 구성됐으며, 이 모델은 만성 B형간염의 간암 예측을 위한 인공지능 기반 모델(prediction of liver cancer using artificial intelligence-driven model with neural network-based software for hepatitis B–deepfore, PLAN-B-DF)로 명명됐다.
PLAN-B-DF 모델의 성능은 내부 검증 코호트에서 c-index 0.91 (95% 신뢰구간 0.89–0.93)을 기록했으며, 외부 검증 코호트에서도 c-index 0.89 (95% 신뢰구간 0.87–0.90)로 우수한 예측력을 보였다. 기존의 간암 발생 예측 모델인 PAGE-B (0.72), REACH-B (0.67), CU-HCC (0.65)와 비교했을 때 PLAN-B-DF는 가장 높은 예측 성능을 나타냈으며, 모든 모델과의 비교에서 통계적으로 유의미한 차이를 보였다. 또한, PLAN-B-DF 모델의 출력값을 통해 간암 발생 위험도를 최소 위험, 저위험, 중위험, 고위험 그룹으로 분류한 결과, 10년째 누적 간암 발생률은 각각 0.0%, 0.4%, 16.0%, 46.2%로 확인됐다. 이 결과를 통해 PLAN-B-DF 모델이 만성 B형간염 환자의 간암 위험도를 정밀하게 분류할 수 있음을 입증했다.
PLAN-B-DF는 인공지능 기계 학습과 영상 바이오마커를 활용해 기존 예측 모델 대비 상당히 높은 예측 정확도를 확보했으며, 기존의 임상 변수 기반 모델보다 정밀한 개별 맞춤형 감시 전략 수립에 기여할 것으로 기대된다. 또한 본 연구를 근거로 향후 영상 바이오마커의 활용 범위를 확장하는 데 기여할 것으로 예상된다. 아울러 본 연구를 통해 만성 B형간염 환자에서도 만성 대사질환 및 여러 체성분 요인을 포함한 대사 인자의 적극적인 조절이 필요함이 확인됐으며, PLAN-B-DF를 활용하여 간암 발생 위험도를 정밀하게 예측하고 개별화된 맞춤 감시 전략을 수립하는 것이 가능할 것으로 기대된다.
Distant origin of glioblastoma recurrence: neural stem cells in the subventricular zone serve as a source of tumor reconstruction after primary resection
Molecular Cancer

(의학과,공동교신저자)

(암연구소,공동제1저자)
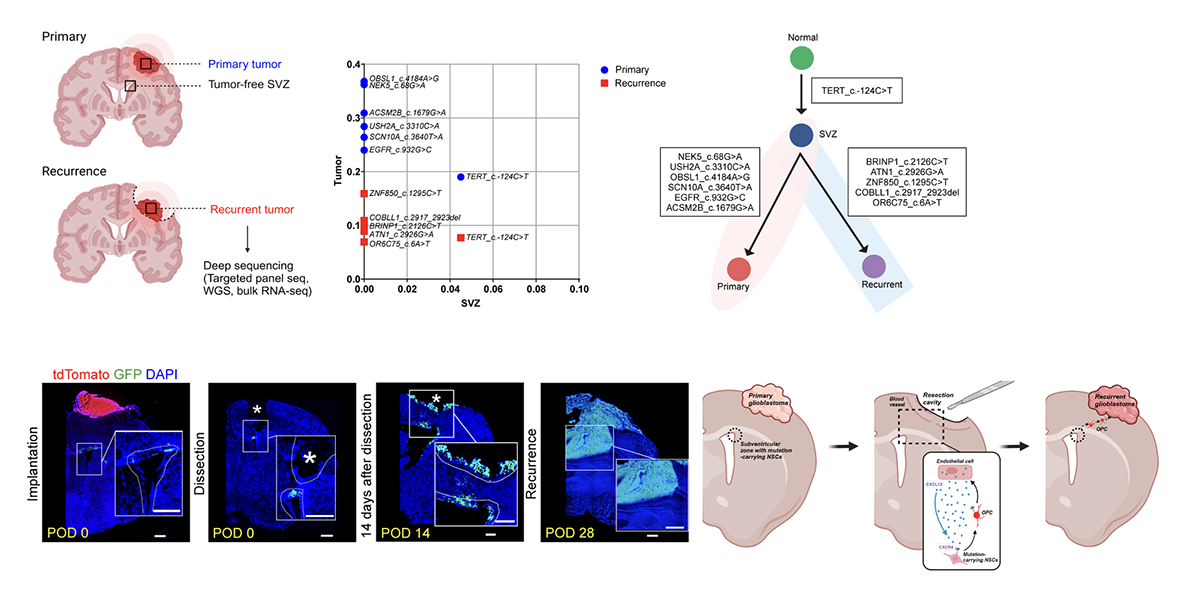
이번 연구는 서울대학교 의과대학 의학과 이주호 교수 연구팀과 연세대학교 신경외과 강석구 교수, 그리고 한국과학기술원 이정호 교수 연구팀이 공동으로 수행한 연구로 암의 재발 과정에서 잔여 암조직뿐만 아니라 원격 부위의 신경줄기세포가 재발의 근원임을 규명하며, 재발 메커니즘에 대한 새로운 가설을 제시하고, 이를 인간 유전체 분석과 동물 모델을 활용하여 증명한 연구이다.
교모세포종은 성인 악성 뇌종양 중 가장 흔한 종양이지만, 적극적인 수술적 절제로 종양을 완전 적출하더라도 대부분 환자에서 수술적 절제 위치에서 재발을 하게 되고, 중앙 생존값 역시 1-2년으로 재발율이 극히 높고 예후가 불량하다. 기존에는 이러한 불량한 치료 성적이 교모세포종의 높은 치료 저항성 때문이라고 여겨, 종양의 완전 제거를 목표로 국소 치료 강도를 높이는 방향으로 연구가 진행되어 왔다.
본 연구팀은 기존에 교모세포종의 세포적 근원이 뇌실하지역의 신경줄기세포임을 밝혔으며, 이를 기반으로 재발암의 발생 과정이 잔여암조직 외에 뇌실하지역의 암유발 줄기세포일 가능성에 대해 가설을 수립하여 연구를 진행했다. 초발-재발 암 조직 및 뇌실하지역의 조직을 수집하여 이에 대한 유전적 계통 관계를 분석한 결과, 재발암의 약 60%가 원발암과 유전적 계통이 분리되어 있음을 확인하였고, 더 나아가 재발암의 유전적 기원이 뇌실하지역임을 밝혔다. 이를 근거로 하여 초발-재발 이중형광을 통한 세포 기원 추적이 가능한 교종 재발 동물모델을 개발하였고, 이를 통해 재발암이 초발암과 관련 없이 신경줄기세포로부터 독립적으로 구성될 수 있음을 발견하였다. 더 나아가 수술 절제 시 절제 부위의 혈관내피세포와 신경줄기 세포 간에 CXCL12-CXCR4 상호작용이 발생하는 것이 재발 기전임을 찾아내어 이를 차단함으로써 신경줄기세포 기반의 재발을 차단하고 동물모델의 생존율이 상승하여 새로운 재발 기전을 차단할 수 있는 신치료전략을 발굴하였다.
이번 연구는 대표적 난치암인 교모세포종의 새로운 재발 기전을 밝혀, 교모세포종 연구의 새로운 분야를 개척하였고, 이를 차단할 수 있는 기전과 전략을 발굴하여 임상 적용 가능성까지 발전시킨 연구로, 서울대학교, 연세대학교, 한국과학기술원 간의 협업을 통해 우수한 연구 성과로 이어질 수 있었다.